题目内容
19.如图是电解CuCl2溶液的装置,其中c、d为石墨电极,下列判断正确的是( )
| A. | c为阴极,d为阳极 | B. | 氯离子往d电极移动 | ||
| C. | 该装置能将化学能转化为电能 | D. | d的电极反应式为:Cu2++2e-═Cu |
分析 在电解池中,电流的流向和电子的移动方向相反,根据电子或电流的流向可以确定电解池的阴阳极,进而确定电极反应.
解答 解:在电解池中,电流的流向和电子的移动方向相反,电流是从正极流向阳极,所以c是阳极,d是阴极,a是正极,b是负极.
A、c是阳极,d是阴极,故A错误;
B、电解过程中,氯离子在阳极c上失电子产生氯气,氯离子浓度减小,所以氯离子往c电极移动,故B错误;
C、该装置能将电能转化为化学能,故C错误;
D、电解过程中,d电极是阴极,该电极上铜离子得电子析出金属铜,电极质量增加,所以电极反应式为:Cu2++2e-═Cu,故D正确.
故选D.
点评 本题考查电解池的工作原理,难度不大,会根据电子流向和电流流向判断电源的正负极,从而确定电极的阴阳极,再根据所学知识进行回答.

练习册系列答案
相关题目
1.下列化学用语正确的是( )
| A. | 乙酸的结构简式:C2H4O2 | B. | 氯化氢的电子式: | ||
| C. | 镁的原子结构示意图: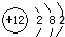 | D. | 水的电离方程式:H2O═H++OH- |
2.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 无色溶液中:Al3+、NH4+、Cl-、HS- | |
| B. | Na2CO3溶液中:K+、NH4+、SO42-、Cl- | |
| C. | 漂白粉的水溶液中:Fe2+、SO42-、Mg2+、Na+ | |
| D. | 水电离出的c(H+)=1×10-13mol•L-1的水溶液中:Ca2+、HCO3-、I-、NO3- |
7.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是( )
| A. | 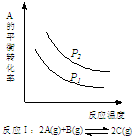 反应:△H>0,P2>P1 | B. | 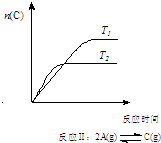 反应:△H<0,T1<T2 | ||
| C. | 反应:△H>0,T2>T1;或△H<0,T2<T1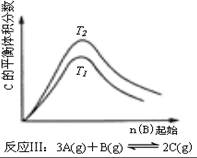 | D. | 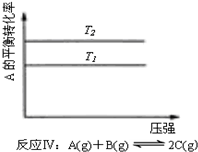 反应:△H<0,T2>T1 |
4.从1897年英国首次使用氯气对给水管网消毒以来,氯气用于自来水消毒已经经历了100多年的历史.目前,我国大多数城市仍然采用氯气消毒法对自来水进行净化、消毒.氯气之所以长期用于自来水消毒,原因是( )
| A. | 氯气有毒,可以毒死细菌、病毒 | |
| B. | 氯气具有刺激性气味,可以熏死细菌、病毒 | |
| C. | 氯气与水反应生成具有强氯化性的HClO,可以杀死细菌、病毒 | |
| D. | 氯气用于自来水消毒没有任何有毒物质残留 |
11.糖类、油脂和蛋白质是维持人体生命活动所必须的三大营养物质,以下叙述正确的是( )
| A. | 淀粉水解的最终产物是葡萄糖 | |
| B. | 植物油不能使溴的四氯化碳溶液褪色 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
9.下列关于硝酸的认识中,正确的是( )
| A. | 浓硝酸和稀硝酸都具有氧化性 | |
| B. | 浓硝酸与金属反应不产生氢气,而稀硝酸与金属反应可置换出氢气 | |
| C. | 因常温下铝和铁不与浓硝酸反应,所以浓硝酸可盛放在铝制或铁制容器中 | |
| D. | 硝酸与金属反应时,只表现出氧化性 |
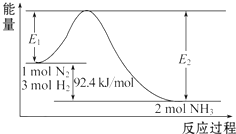 科学家一直致力于“人工固氮”的方法研究.
科学家一直致力于“人工固氮”的方法研究.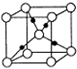 已知A、B、C、D、E、F、G、H均为前四周期元素且原子序数依次增大,A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;元素C的基态原子2p轨道有3个未成对电子,元素D的原子最外层电子数是其内层电子数的3倍,元素F的一种常见单质为淡黄色粉末,G的内层轨道全部排满电子,且最外层电子数为1.E是地壳中含量最高的金属元素;H与E同主族.
已知A、B、C、D、E、F、G、H均为前四周期元素且原子序数依次增大,A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;元素C的基态原子2p轨道有3个未成对电子,元素D的原子最外层电子数是其内层电子数的3倍,元素F的一种常见单质为淡黄色粉末,G的内层轨道全部排满电子,且最外层电子数为1.E是地壳中含量最高的金属元素;H与E同主族.