题目内容
当Mg(OH)2在水中达到溶解平衡时:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是( )
| A、NH4Cl |
| B、NaOH |
| C、Na2CO3 |
| D、Fe |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:根据平衡移动原理及溶度积解答,要使Mg (OH)2 固体进一步溶解,即平衡向右移动,可以加水,或降低Mg2+或OH-的浓度.
解答:
解:A、加入少量NH4Cl,NH4+与OH-结合生成氨水,故氢氧根的浓度减小,故平衡右移,故A正确;
B、加入NaOH,OH-的浓度增大,平衡向左移动,Mg (OH)2 固体的量增大,故B错误;
C、加入少量Na2C03,CO32-水解生成氢氧根,致使氢氧根浓度增大,平衡左移,Mg (OH)2 固体的量增大,故C错误;
D、加入少量Fe,Fe不溶于水,为金属固体,不改变各种物质的浓度,故D错误;
故选A.
B、加入NaOH,OH-的浓度增大,平衡向左移动,Mg (OH)2 固体的量增大,故B错误;
C、加入少量Na2C03,CO32-水解生成氢氧根,致使氢氧根浓度增大,平衡左移,Mg (OH)2 固体的量增大,故C错误;
D、加入少量Fe,Fe不溶于水,为金属固体,不改变各种物质的浓度,故D错误;
故选A.
点评:本题考查化学平衡的移动,难度不大,注意D选项中铁单质的溶解性以及对溶液中离子浓度的影响.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
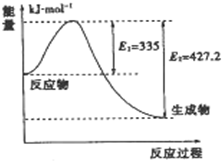 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.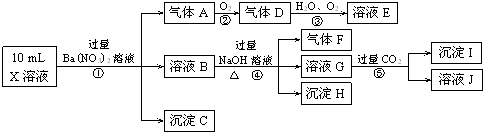
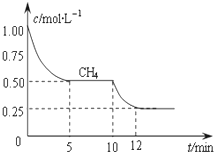 合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有:
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有:
