题目内容
15.检验牙膏中是否含有甘油选用的试剂是( )| A. | 氢氧化钠溶液 | B. | 氢氧化铜浊液 | C. | 醋酸溶液 | D. | 碳酸钠溶液 |
分析 甘油含有羟基,与氢氧化钠、碳酸钠等不反应,可与氢氧化铜浊液发生颜色反应,以此解答该题.
解答 解:甘油为多羟基醇,遇新制氢氧化铜呈现绛蓝色,与氢氧化钠、碳酸钠等不反应,一般条件下与醋酸不反应,只有B正确.
故选B.
点评 本题考查有机物的检验,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及反应现象的判断,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列关于有机物的认识正确的是( )
| A. | 淀粉、油脂、蛋白质在氧气中充分燃烧,均只生成CO2和H2O | |
| B. | 分子组成为CH4和C2H6O的有机物都不存在同分异构现象 | |
| C. | 乙醇与氧气在不同条件下反应,可以得到不同产物 | |
| D. | 乙烯使溴的四氯化碳溶液褪色是因为发生了取代反应 |
6.设NA表示阿伏加德罗常数,下列叙述中,正确的是( )
| A. | 25℃、101kPa时,11.2L H2中含有的原子数为NA | |
| B. | 78g Na2O2与足量水充分反应时电子转移数为2NA | |
| C. | 等质量的CO与CO2中所含碳原子数之比为11:7 | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L |
20.某同学根据H2S和浓H2SO4的性质做出下列推测,其中正确的是( )
| A. | 浓H2SO4具有强氧化性是因为其中含+6价S,所有只要含最高价+6价S的化合物就具有强氧化性 | |
| B. | H2S中的S处于最低价,因此其不可能具有氧化性 | |
| C. | 浓H2SO4可把Na2SO3氧化 | |
| D. | 因为元素化合价变化以相邻价态之间转化最容易,因此发生氧化还原反应时,浓H2SO4对应的产物一般为SO2 |
7.关于溶液、胶体和浊液三种分散系,下列叙述中不正确的是( )
| A. | 丁达尔现象可用来区分AgI胶体和FeCl3溶液 | |
| B. | 静置片刻后,Fe(OH)3胶体中会出现分层现象 | |
| C. | 溶液、胶体、浊液的根本区别是分散质粒子直径的大小 | |
| D. | 胶体的主要性质有:丁达尔现象、电泳、聚沉等 |
4.下列化学方程式错误的是( )
| A. | Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑ | B. | MgCO3+CO2+H2O═Mg(HCO3)2 | ||
| C. | MgCO3+H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑ | D. | CaCO3+H2O═Ca(OH)2+CO2↑ |
5.下列说法不正确的是( )
| A. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来,金属铝的熔点较低 | |
| B. | 铝与Fe2O3发生铝热反应后固体的质量不变 | |
| C. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | Al、HCl、NaOH中任意两种物质在一定条件下均能发生反应 |

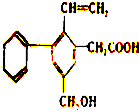 某有机物的结构简式如图所示试回答:
某有机物的结构简式如图所示试回答: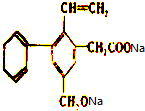 +H2↑.
+H2↑.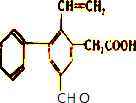 +2H2O.
+2H2O.