题目内容
在2L密闭容器中,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K= .已知:K(300℃)>K(350℃),该反应△H 0,△S 0(填“>”、“<”或“=”).
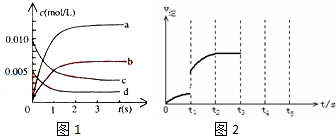
(2)图中表示NO2的变化的曲线是 .用O2表示从0~2s内该反应的平均速率v= .
(3)能说明该反应已经达到平衡状态的是 .
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 .
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效的催化剂
(5)该反应的逆反应速率随时间变化情况如下图所示.从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是 (填序号)
a.升温
b.增大O2的浓度
c.使用催化剂
d.增压.

| 时间(S) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的变化的曲线是
(3)能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效的催化剂
(5)该反应的逆反应速率随时间变化情况如下图所示.从图中看到,反应在t2时达平衡,在t1时改变了某种条件,改变的条件可能是
a.升温
b.增大O2的浓度
c.使用催化剂
d.增压.
考点:化学平衡常数的含义,化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)依据化学方程式结合平衡常数概念书写平衡常数表达式;温度越高,平衡常数越小说明平衡逆向进行程度越大;正反应是气体物质的量减少的反应;
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO);根据v=
计算v(NO),再利用速率之比等于化学计量数之比计算v(O2);
(3)可逆反应达到平衡时,v正=V逆 (同种物质表示)或正逆速率之比等于化学计量数之比(不同物质表示),反应混合物各组分的物质的量、浓度、含量不再变化,以及由此衍生的一些量也不发生变化,由此进行判断;
(4)为使该反应的反应速率增大,可采用增大压强、升高温度、加入催化剂、增大反应物浓度等方法,再结合平衡移动原理分析解答;
(5)根据影响化学反应速率的因素来确定改变的条件.
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO);根据v=
| △c |
| △t |
(3)可逆反应达到平衡时,v正=V逆 (同种物质表示)或正逆速率之比等于化学计量数之比(不同物质表示),反应混合物各组分的物质的量、浓度、含量不再变化,以及由此衍生的一些量也不发生变化,由此进行判断;
(4)为使该反应的反应速率增大,可采用增大压强、升高温度、加入催化剂、增大反应物浓度等方法,再结合平衡移动原理分析解答;
(5)根据影响化学反应速率的因素来确定改变的条件.
解答:
解:(1)2NO(g)+O2(g)═2NO2(g),依据化学方程式写出平衡常数表达式为:
;K300°C>K350°C,说明温度越高平衡常数越小,平衡逆向进行,逆向是吸热反应,正向是放热反应,则该反应是放热反应,物质的是减小的反应,所以△S>0,
故答案为:
;<;<;
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO)=
=0.0065mol/L,所以图中表示NO2变化的曲线是b,
2s内用NO表示的平均反应速率v(NO)=
=
=3.0×10-3mol?L-1?s-1,速率之比等于化学计量数之比,
所以v(O2)=
v(NO)=
×3.0×10-3mol?L-1?s-1=1.5×10-3mol?L-1?s-1,
故答案为:b;1.5×10-3mol?L-1?s-1;
(3)2NO(g)+O2(g)═2NO2(g),反应是气体体积减小的放热反应
a、v(NO2)=2v(O2) 表示同一方向反应速率,v(NO2)自始至终为v(O2)的2倍,不能说明达到平衡,故a错误;
b、随反应进行,反应混合气体总的物质的量在减小,压强之比等于气体物质的量之比,气体压强保持不变,说明反应到达平衡,故b正确;
c、v逆(NO)=2v逆(O2)=2v正(O2),说明反应达到平衡状态,故c正确;
d、反应前后气体质量守恒,体积不变,反应过程中和平衡状态下,气体密度都不变,所以不能说明反应达到平衡状态,故d错误;
故答案为:bc;
(4)a.及时分离除NO2气体平衡向右移动,但反应速率减小,故错误;
b.适当升高温度,反应速率增大但平衡向逆反应方向移动,故错误;
c.增大O2的浓度反应速率增大,且该反应向正反应方向移动,故正确;
d.选择高效催化剂能增大反应速率,但平衡不移动,故错误;
故选c;
(5)从如图可知,在t1时改变了某种反应条件,反应在t2时达到平衡,改变的条件使速率变化离开原速率点了,应该是同时能让正逆反应速率加快的条件,
a.升温,正逆反应速率都加快,逆向移动,故错误;
b.增大O2的浓度,逆速率无变化不离开原速率点,故错误;
c.使用催化剂,平衡不移动,故错误;
d.增压,正逆速率都加快,正向移动,故正确;
故答案为:d.
| c2(NO2) |
| c2(NO)c(O2) |
故答案为:
| c2(NO2) |
| c2(NO)c(O2) |
(2)NO2是产物,随反应进行浓度增大,平衡时浓度为NO浓度的变化量△c(NO)=
| 0.020mol-0.007mol |
| 2L |
2s内用NO表示的平均反应速率v(NO)=
| ||
| △t |
| ||
| 2s |
所以v(O2)=
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:b;1.5×10-3mol?L-1?s-1;
(3)2NO(g)+O2(g)═2NO2(g),反应是气体体积减小的放热反应
a、v(NO2)=2v(O2) 表示同一方向反应速率,v(NO2)自始至终为v(O2)的2倍,不能说明达到平衡,故a错误;
b、随反应进行,反应混合气体总的物质的量在减小,压强之比等于气体物质的量之比,气体压强保持不变,说明反应到达平衡,故b正确;
c、v逆(NO)=2v逆(O2)=2v正(O2),说明反应达到平衡状态,故c正确;
d、反应前后气体质量守恒,体积不变,反应过程中和平衡状态下,气体密度都不变,所以不能说明反应达到平衡状态,故d错误;
故答案为:bc;
(4)a.及时分离除NO2气体平衡向右移动,但反应速率减小,故错误;
b.适当升高温度,反应速率增大但平衡向逆反应方向移动,故错误;
c.增大O2的浓度反应速率增大,且该反应向正反应方向移动,故正确;
d.选择高效催化剂能增大反应速率,但平衡不移动,故错误;
故选c;
(5)从如图可知,在t1时改变了某种反应条件,反应在t2时达到平衡,改变的条件使速率变化离开原速率点了,应该是同时能让正逆反应速率加快的条件,
a.升温,正逆反应速率都加快,逆向移动,故错误;
b.增大O2的浓度,逆速率无变化不离开原速率点,故错误;
c.使用催化剂,平衡不移动,故错误;
d.增压,正逆速率都加快,正向移动,故正确;
故答案为:d.
点评:本题考查了化学平衡影响因素、平衡标志分析判断,平衡常数、反应速率的计算应用,掌握基础和移动原理是关键,题目难度中等.

练习册系列答案
相关题目
下列实验操作方法不正确的是( )
| A、试管内壁附着的硫黄可以用热的KOH溶液洗涤,也可以用CS2洗涤 |
| B、盛Na2SO3、Na2S、KI溶液的试剂瓶不能用玻璃塞,贮存时应盖好瓶塞,防止被空气氧化 |
| C、金属镁着火可用干粉灭火器灭火,也可用泡沫灭火器灭火 |
| D、从硫酸铜溶液中获取硫酸铜晶体,可以用蒸发结晶,也可以用冷却结晶 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、饱和氯水中:NH4+、SO32-、SO42-、Cl- |
| C、与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
| D、c(H+)=1.0×10-13mol/L溶液中:K+、Na+、CH3COO-、Br- |
下列反应最终能生成Fe3+的化合物的是( )
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
| A、①②③ | B、①③⑤ |
| C、③④ | D、③⑤ |
下列物质露置在空气中质量会减轻的是( )
| A、浓盐酸 |
| B、Na2O2 |
| C、NaOH |
| D、浓硫酸 |
某无色溶液既可能是强酸性又可能是强碱性,在该溶液中一定能大量共存的离子是( )
| A、H+ Na+ NO3- SO42- |
| B、Na+ CO32- Cu2+ Cl- |
| C、K+ Na+ Cl- SO42- |
| D、K+ Cl- Ba2+ HCO3- |
采用NH3作还原剂,除去烟气中的氮氧化物,反应原理为:NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g).如图是烟气以固定的流速通过两种不同催化剂①和②时,测量相同时间得到的烟气脱氮率图象.根据该图象,下列说法中正确的是( )
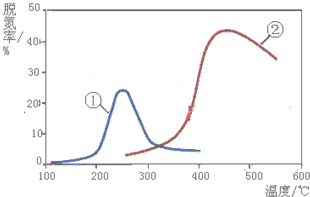

| A、上述反应的正反应为吸热反应 |
| B、催化剂①、②分别适合于250℃和450℃左右脱氮 |
| C、催化剂②比①脱氮效果好,说明催化剂②能导致该反应平衡向右移动程度更大 |
| D、相同条件下,改变压强对脱氮率没有影响 |
 如图为直流电源电解稀Na2SO4溶液的装置.通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液.则下列有关说法中正确的是( )
如图为直流电源电解稀Na2SO4溶液的装置.通电一段时间后,在石墨电极a和b附近分别滴加一滴酚酞溶液.则下列有关说法中正确的是( )| A、a电极产生H2 |
| B、两极产生的气体均有刺激性气味 |
| C、通电一段时间后,稀Na2SO4溶液酸性增强 |
| D、a电极附近呈无色,b电极附近呈红色 |