题目内容
用下列装置能实现相应实验目的是( )
A、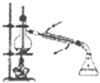 石油的蒸馏 |
B、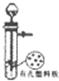 用大理石和稀盐酸制备CO2 |
C、 滴定管读数 |
D、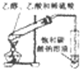 醋化反应 |
考点:化学实验方案的评价
专题:
分析:A.蒸馏时测定馏分的温度,水要下进上出;
B.大理石为块状固体,与盐酸反应生成二氧化碳,图中装置可使反应随时停止;
C.滴定管读数要准确到0.01mL;
D.催化剂选择不合理,导气管在液面下,发生倒吸.
B.大理石为块状固体,与盐酸反应生成二氧化碳,图中装置可使反应随时停止;
C.滴定管读数要准确到0.01mL;
D.催化剂选择不合理,导气管在液面下,发生倒吸.
解答:
解:A.图中温度计位置、水流方向不合理,蒸馏时温度计水银球应在蒸馏烧瓶的支管口处,水要下进上出,故A错误;
B.大理石为块状固体,与盐酸反应生成二氧化碳,关闭止水夹可使反应随时停止,制备装置合理,故B正确;
C.滴定管读数要准确到0.01mL,图中读数不合理,故C错误;
D.催化剂选择不合理,导气管在液面下,发生倒吸,则应利用浓硫酸作催化剂、吸水剂,导气管在液面以上,故D错误;
故选B.
B.大理石为块状固体,与盐酸反应生成二氧化碳,关闭止水夹可使反应随时停止,制备装置合理,故B正确;
C.滴定管读数要准确到0.01mL,图中读数不合理,故C错误;
D.催化剂选择不合理,导气管在液面下,发生倒吸,则应利用浓硫酸作催化剂、吸水剂,导气管在液面以上,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯实验、气体的制取、有机物的制备及滴定实验等,把握物质性质、化学实验基本操作等为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
向200mL1.5mol?L-1的硫酸溶液中加入一定量Fe2O3、Cu的混合物,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,剩余固体的质量为( )
| A、17.6g | B、22.4g |
| C、2.4g | D、4.8g |
质量分数相等的Na2CO3和NaHCO3混合物xg,加热一段时间后质量变为yg,当y为何值时,表明NaHCO3完全分解( )
A、
| ||
B、
| ||
C、
| ||
D、
|
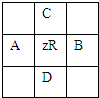 有原子序数为Z的元素R,在周期表中位于A、B、C、D四种元素中间,如图所示,
有原子序数为Z的元素R,在周期表中位于A、B、C、D四种元素中间,如图所示,A、B、C、D四种元素的原子序数之和不可能是( )
| A、4Z | B、4Z+10 |
| C、4Z+5 | D、4Z+14 |
下列化学实验事实及其结论正确的是( )
| A、向碘水中滴加CCl4,振荡后静置,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| B、Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| C、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| D、高温下,用金属钠与氯化钾可以置换出金属钾,说明钠的金属性比钾强 |
将一定量的NaHCO3和Na2O2的混合物置于一密闭容器中充分加热,反应中转移的电子数为1mol,下列说法一定正确的是( )
| A、混合物中NaHCO3和Na2O2物质的量一定相等 |
| B、容器中肯定有0.5molO2 |
| C、反应后,容器中的固体只有Na2CO3 |
| D、反应后,容器中一定没有H2O |