题目内容
既能与H+ 反应又能与OH-反应的离子是( )
| A、Al3+ |
| B、AlO2- |
| C、Fe3+ |
| D、HCO3- |
考点:两性氧化物和两性氢氧化物
专题:元素及其化合物
分析:Al3+、Fe3+能与OH-反应,不与H+反应,AlO2-能与H+反应,不能与OH-反应,碳酸氢根为弱酸酸式酸根,能与酸、碱反应.
解答:
解:A.Al3+能与OH-反应生成氢氧化铝沉淀或偏铝酸盐,不与H+反应,故A不选;
B.AlO2-能与H+反应得到氢氧化铝沉淀或铝盐,不能与OH-反应,故B不选;
C.Fe3+能与OH-反应生成氢氧化铁沉淀,不与H+反应,故C不选;
D.HCO3-能与OH-反应得到碳酸根,能与H+反应生成二氧化碳,故D选;
故选:D.
B.AlO2-能与H+反应得到氢氧化铝沉淀或铝盐,不能与OH-反应,故B不选;
C.Fe3+能与OH-反应生成氢氧化铁沉淀,不与H+反应,故C不选;
D.HCO3-能与OH-反应得到碳酸根,能与H+反应生成二氧化碳,故D选;
故选:D.
点评:本题考查元素化合物性质,比较基础,侧重考查常见离子的反应,题目难度不大.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
下列叙述正确的是( )
| A、向次氯酸钠溶液中通入足量SO2气体的离子方程式:ClO-+SO2+H2O→HClO+HSO3- |
| B、向明矾溶液中加入过量NaOH 溶液会产生大量白色沉淀 |
| C、铁粉与足量稀硝酸反应时,氧化剂与还原剂的物质的量之比为2:3 |
| D、浓硫酸、浓硝酸在加热条件下都能将木炭氧化为二氧化碳 |
甲、乙、丙三种元素均位于第三周期,其原子序数逐渐增大,甲的最高价氧化物对应的水化物是强碱,乙是地壳中含量最多的金属元素,丙是本周期中原子半径最小的元素.下列说法不正确的是( )
| A、甲是第ⅠA元素,丙是第VⅡA元素 |
| B、甲、丙形成的化合物是离子化合物 |
| C、乙的最高价氧化物是两性氧化物 |
| D、丙是元素周期表中非金属性最强的元素 |
下列化合物分别与金属钠反应,其中反应最慢的是( )
| A、CH3CH2OH |
| B、CH3COOH |
| C、H2O |
| D、C6H5OH |
下列物质中,一定属于同系物的是( )
| A、C2H4 C2H6 |
| B、C2H6 C3H8 |
| C、CH4、C2H4 |
| D、C2H4、C3H4 |
下列各项操作中不发生先沉淀后溶解现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量H2SO4
③向Ba(NO3)2溶液中通入过量SO3
④向石灰水中通入过量CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸.
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量H2SO4
③向Ba(NO3)2溶液中通入过量SO3
④向石灰水中通入过量CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸.
| A、①②③ | B、①②⑤ |
| C、①②③⑤ | D、①③⑤ |
下列判断正确的是( )
| A、Na2S2O3溶液中加入稀硫酸的离子方程式为:2S2O32-+4H+═SO42-+3S↓+2H2O |
| B、用TiCl4制备TiO2的反应可表示为:TiCl4+(x+2)H2O(过量)═TiO2?xH2O↓+4HCl |
| C、滴加甲基橙试液后呈红色的溶液中可以大量共存:Na+、CO32-、K+、AlO2- |
| D、25℃时,pH=12的NaOH溶液中含有OH-的数目为0.01NA |
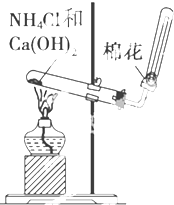 如图是实验室制取的气体发生装置,请结合所学知识,回答下列问题:
如图是实验室制取的气体发生装置,请结合所学知识,回答下列问题: