题目内容
(1)使1mol 1,3-丁二烯(CH2=CH-CH=CH2)与氯气完全发生加成反应,然后使该加成反应的产物与氯气在光照条件下发生取代反应,则两个过程中消耗氯气的总物质的量最多为 .
(2)1mol 与足量氢气发生加成反应,消耗氢气的物质的量为 .
与足量氢气发生加成反应,消耗氢气的物质的量为 .
(3)标准状况下2.24L无色可燃气体在足量氧气中完全燃烧.若将产物通入足量无水氯化钙固体,无水氯化钙质量增加5.4g;若用足量碱石灰吸收燃烧产物,质量增加14.2g.若原气体是单一烃类气体,则它的分子式是: .
(4)某有机物含碳85.7%,含氢14.3%,向160g含溴10%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总重164.2g.求:有机物分子式 .
(5)在甲醛(CH2O)、乙醛和乙酸乙酯组成的混合物中,氢元素的质量分数是8%,则氧元素的质量分数为 .
(6)常温常压下,20mL某气态烃与同温同压下的过量氧气70mL混合,点燃爆炸后,恢复到原来状况,其体积为50mL,求此烃可能有的分子式: .(只需写出其中一种情况即可)
(2)1mol
 与足量氢气发生加成反应,消耗氢气的物质的量为
与足量氢气发生加成反应,消耗氢气的物质的量为(3)标准状况下2.24L无色可燃气体在足量氧气中完全燃烧.若将产物通入足量无水氯化钙固体,无水氯化钙质量增加5.4g;若用足量碱石灰吸收燃烧产物,质量增加14.2g.若原气体是单一烃类气体,则它的分子式是:
(4)某有机物含碳85.7%,含氢14.3%,向160g含溴10%的溴水中通入该有机物,溴水恰好完全褪色,此时液体总重164.2g.求:有机物分子式
(5)在甲醛(CH2O)、乙醛和乙酸乙酯组成的混合物中,氢元素的质量分数是8%,则氧元素的质量分数为
(6)常温常压下,20mL某气态烃与同温同压下的过量氧气70mL混合,点燃爆炸后,恢复到原来状况,其体积为50mL,求此烃可能有的分子式:
考点:消去反应与水解反应,化学方程式的有关计算,有机物实验式和分子式的确定
专题:有机反应,有机物分子组成通式的应用规律
分析:(1)1,3-丁二烯和氯气发生加成反应需要2mol的氯气;
有机物中的氢原子被氯原子取代时,氯气的物质的量与取代的氢原子的物质的量相等,所以最多消耗的氯气为这两部分之和;
(2)双键和氢气按1:1加成,苯环和氢气按1:3加成;
(3)无水氯化钙质量增重5.4g为水的质量,碱石灰质量增加14.2g为水和二氧化碳的质量,可计算出02.24L气态烃含有的C、H原子数,进而计算分子式;
(4)液体增重为:164.2g-160g=4.2g,为有机物的质量,根据碳氢质量分数可计算实验式,根据溴的量可知烃的量,计算出烃的摩尔质量结合实验式计算分子式;
(5)在甲醛(HCHO)、乙醛(CH3CHO)和乙酸乙酯(C4H8O2)组成的混合物中,C、H两种元素的原子个数始终是1:2,故C、H两元素的质量之比=12:2=6:1,根据氢元素质量计算C元素的质量分数,根据ω(O)=1-ω(C)-ω(H)计算;
(6)该烃完全燃烧,完全燃烧发生反应CxHy+(x+
)O2→xCO2+
H2O(l),则(x+
)<
=3.5,根据反应前后气体的体积变化,用差量法进行计算,注意生成的水为液体.
有机物中的氢原子被氯原子取代时,氯气的物质的量与取代的氢原子的物质的量相等,所以最多消耗的氯气为这两部分之和;
(2)双键和氢气按1:1加成,苯环和氢气按1:3加成;
(3)无水氯化钙质量增重5.4g为水的质量,碱石灰质量增加14.2g为水和二氧化碳的质量,可计算出02.24L气态烃含有的C、H原子数,进而计算分子式;
(4)液体增重为:164.2g-160g=4.2g,为有机物的质量,根据碳氢质量分数可计算实验式,根据溴的量可知烃的量,计算出烃的摩尔质量结合实验式计算分子式;
(5)在甲醛(HCHO)、乙醛(CH3CHO)和乙酸乙酯(C4H8O2)组成的混合物中,C、H两种元素的原子个数始终是1:2,故C、H两元素的质量之比=12:2=6:1,根据氢元素质量计算C元素的质量分数,根据ω(O)=1-ω(C)-ω(H)计算;
(6)该烃完全燃烧,完全燃烧发生反应CxHy+(x+
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |
| 70 |
| 20 |
解答:
解:(1)1,3-丁二烯和氯气发生加成反应需要2mol的氯气,加成产物与氯气发生取代反应,最多需要6mol氯气,
这两部分之和为2mol+6mol=8mol;
故答案为:8;
(2)此结构中含3mol双键,需3mol氢气,苯环需3mol氢气,共需6mol氢气;
故答案为:6mol;
(3)无水氯化钙质量增重5.4g为水的质量,n(H2O)=
=0.3mol,碱石灰质量增加14.2g为水和二氧化碳的质量,含二氧化碳质量为:14.2g-5.4g=8.8g,含二氧化碳的物质的量为:
=0.2mol,2.24L烃的物质的量为:
=0.1mol,故1mol该烃中含碳2mol,含氢6mol,分子式为:C2H6,故答案为:C2H6;
(4)液体增重为:164.2g-160g=4.2g,为有机物的质量,160g含溴10%的溴水中含溴16g,物质的量为:
=0.1mol,N(C):N(H)
:
=7.14:14.3=1:2,该烃实验式为:CH2,为烯烃,160g含溴10%的溴水中含溴16g,物质的量为:
=0.1mol,和该烃恰好反应,故该烯烃的物质的量为0.1mol,该烃的摩尔质量为:
=42g/mol,设分子式为:CnH2n,则14n=42,n=3,故分子式为:C3H6;
故答案为:C3H6;
(5)在甲醛(HCHO)、乙醛(CH3CHO)和乙酸乙酯(C4H8O2)混合物中,碳原子与氢原子个数之比为1:2,则碳元素与氢元素的质量之比为12:2=6:1,混合物中氢元素质量分数为8%,则C元素的质量分数为8%×6=48%,故混合物中氧元素的质量分数为1-48%-8%=44%,
故答案为:44%;
(6)该烃的分子式为CxHy,烃燃烧生成液态水,则:
CxHy+(x+
)O2→xCO2+
H2O(l) 体积减小
1 1+
20mL 20mL+70mL-50mL=40mL
所以,1:(1+
)=20mL:40mL,解得y=4,
完全燃烧,则(x+
)<
=3.5,所以x<3.5,故x=1或2或3,故该烃为CH4 或C2H4或C3H4 ,
故答案为:CH4 或C2H4或C3H4.
这两部分之和为2mol+6mol=8mol;
故答案为:8;
(2)此结构中含3mol双键,需3mol氢气,苯环需3mol氢气,共需6mol氢气;
故答案为:6mol;
(3)无水氯化钙质量增重5.4g为水的质量,n(H2O)=
| 5.4g |
| 18g/mol |
| 8.8g |
| 44g/mol |
| 2.24L |
| 22.4L/mol |
(4)液体增重为:164.2g-160g=4.2g,为有机物的质量,160g含溴10%的溴水中含溴16g,物质的量为:
| 16g |
| 160g/mol |
| 85.7% |
| 12 |
| 14.3% |
| 1 |
| 16g |
| 160g/mol |
| 4.2g |
| 0.1mol |
故答案为:C3H6;
(5)在甲醛(HCHO)、乙醛(CH3CHO)和乙酸乙酯(C4H8O2)混合物中,碳原子与氢原子个数之比为1:2,则碳元素与氢元素的质量之比为12:2=6:1,混合物中氢元素质量分数为8%,则C元素的质量分数为8%×6=48%,故混合物中氧元素的质量分数为1-48%-8%=44%,
故答案为:44%;
(6)该烃的分子式为CxHy,烃燃烧生成液态水,则:
CxHy+(x+
| y |
| 4 |
| y |
| 2 |
1 1+
| y |
| 4 |
20mL 20mL+70mL-50mL=40mL
所以,1:(1+
| y |
| 4 |
完全燃烧,则(x+
| y |
| 4 |
| 70 |
| 20 |
故答案为:CH4 或C2H4或C3H4.
点评:本题考查了反应类型和实验式和分子式的确定,较基础,注意在计算元素含量时,要巧妙运用分子式解答.

练习册系列答案
相关题目
下面有关Na2CO3与NaHCO3的性质比较中错误的是( )
| A、热稳定性:Na2CO3>NaHCO3 |
| B、相同浓度溶液的碱性:Na2CO3>NaHCO3 |
| C、相同温度下在水中的溶解度:Na2CO3>NaHCO3 |
| D、相同条件下与酸反应的剧烈程度:Na2CO3>NaHCO3 |
下列与实验相关的叙述正确的是( )
| A、将FeCl3稀溶液加热蒸发浓缩制备FeCl3的浓溶液 |
| B、做氢气还原氧化铜的实验是,应先通氢气后加热氧化铜 |
| C、稀释浓硫酸时,应将蒸馏水沿烧杯内壁缓慢地注入浓硫酸中并不断搅拌 |
| D、配制1 mol?L-1350mLNaCl溶液可以选择一个100mL的容量瓶和一个250 mL的容量瓶 |
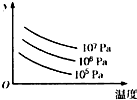 某密闭容器中,发生可逆反应L(s)+G(g)?3R(g)△H>0,如图表示温度、压强的变化对上述反应的影响.下列表述正确的是( )
某密闭容器中,发生可逆反应L(s)+G(g)?3R(g)△H>0,如图表示温度、压强的变化对上述反应的影响.下列表述正确的是( )| A、该反应达到平衡后加入适当的催化剂可提高G的转化率 |
| B、图中的y可能是达到平衡时G的转化率 |
| C、图中的y可能是平衡时混合气体中G的质量分数 |
| D、平衡后向容器中加入少量L,平衡右移,G的转化率增大 |
一定条件下存在反应:CO(g)+H2O(g)?CO2(g)+H2(g),其正反应放热.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol CO和1mol H2O,在Ⅱ中充入1mol CO2和1mol H2,在Ⅲ中充入2mol CO和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中CO的物质的量比容器Ⅱ中的多 |
| D、容器Ⅰ中CO的物质的量比容器Ⅱ中的少 |
下列关于有机物的性质的叙述正确的是( )
| A、蔗糖和麦芽糖都属于二糖,它们互为同分异构体 |
| B、乙烯和苯都不属于饱和烃,都能使酸性高锰酸钾溶液褪色 |
| C、金属钠与乙醇、乙酸都能反应产生氢气,是因为它们所含的官能团相同 |
| D、工业上经氧化、萃取等方法提取海水中的溴,萃取时可以使用裂化汽油等有机溶剂 |
下列烷烃进行一氯取代反应后,生成三种沸点不同的产物的是( )
| A、(CH3)2CHCH2CH2CH3 |
| B、(CH3CH2)2CHCH3 |
| C、(CH3)3CCH2CH3 |
| D、(CH3)2CHCH(CH3)2 |
生活中处处有化学,请根据你所学过的化学知识,判断下列说法中错误的是( )
| A、抗酸药三硅酸镁的化学式为2MgO?3SiO2?nH2O |
| B、缺铁会引起骨质疏松症 |
| C、磺胺类药物是最早用于治疗全身性感染的人工合成抗菌药 |
| D、钡餐的主要成份为硫酸钡 |
有Fe2+、NO3-、Fe3+、NH4+、H+、和H2O 六种微粒,分别属于同一氧化还原反应的反应物和生成物,且Fe2+Fe3+,下列说法中不正确的是( )
| A、氧化剂和还原剂物质的量之比为1:8 |
| B、该过程说明Fe(NO3)2溶液不宜加酸酸化 |
| C、若有1mol NO3- 发生氧化反应,则转移8mol电子 |
| D、若该反应HNO3参加,则HNO3表现氧化性和酸性 |