题目内容
将11.9gMg、Al、Fe组成的合金溶于足量的NaOH溶液中合金质量减少了2.7g,另取等质量的合金溶于过量稀硝酸中,生成了气体NO,向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全沉淀,其质量为27.2g,则生成气体的体积为(标准状况下)( )
| A、6.72L | B、4.48L |
| C、3.36L | D、无法确定 |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,向反应后的溶液中加入适量NaOH溶液,使Mg2+、Al3+、Fe3+完全沉淀,其质量为27.2g,所得沉淀为氢氧化铁、氢氧化镁、氢氧化铝,由电荷守恒可知,反应中金属铁、铝、镁提供的电子的物质的量等于生成碱的氢氧根离子的物质的量,沉淀的质量等于Fe、Al、Mg的总质量与氢氧根质量之和,从而求出反应中金属铁、Al、Mg失去电子的物质的量;
设生成 NO的标准状况下的体积为V,则有:
×3=合金失去的电子总的物质的量.
设生成 NO的标准状况下的体积为V,则有:
| V |
| 22.4mol/L |
解答:
解:将合金溶于过量稀硝酸中,分别生成Al3+、Fe3+、Mg2+离子,向反应后的溶液中加入量NaOH溶液,使Mg2+、Al3+、Fe3+完全沉淀,其质量为27.2g,所得沉淀为氢氧化铁、氢氧化镁、氢氧化铝,由电荷守恒可知,反应中金属铁、铝、镁提供的电子的物质的量等于生成碱的氢氧根离子的物质的量,沉淀的质量等于Fe、Al、Mg的总质量与氢氧根质量之和,从而求出反应中金属铁、Al、Mg失去电子的物质的量;
设反应中金属铁、铜、Al提供的电子的物质的量为xmol,根据沉淀的质量等于Fe、Cu、Al的总质量与氢氧根质量之和可得:
11.9g+xmol×17g/mol=27.2g,解得x=0.9mol,
因此11.9g合金失去的电子总的物质的量为0.9mol,
设设生成 NO的标准状况下的体积为V,则有:
×3=0.9mol,
解得V=6.72L,
故选A.
设反应中金属铁、铜、Al提供的电子的物质的量为xmol,根据沉淀的质量等于Fe、Cu、Al的总质量与氢氧根质量之和可得:
11.9g+xmol×17g/mol=27.2g,解得x=0.9mol,
因此11.9g合金失去的电子总的物质的量为0.9mol,
设设生成 NO的标准状况下的体积为V,则有:
| V |
| 22.4mol/L |
解得V=6.72L,
故选A.
点评:本题考查金属混合物的计算,难度中等,利用方程式计算步骤繁琐,本题采取守恒方法解答,判断金属提供的电子的物质的量等于氢氧根的物质的量是该方法的关键,注意化合物计算中守恒思想的运用.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
mg铁粉与含有H2SO4的CuSO4溶液完全反应后,得到mg铜,则参与反应的CuSO4与H2SO4的物质的量之比为( )
| A、7:1 | B、1:7 |
| C、7:8 | D、8:7 |
下列实验方案或操作可行的是( )
| A、将水沿着烧杯内壁注入浓硫酸中配制稀硫酸 |
| B、可用分液漏斗分离碘和四氯化碳 |
| C、将O2和H2的混合气体通过灼热的铜网以除去其中的O2 |
| D、将饱和的FeCl3溶液滴入沸水中加热至溶液呈红褐色即可制得Fe(OH)3胶体 |

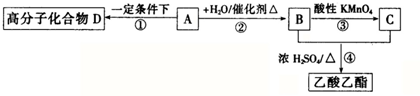

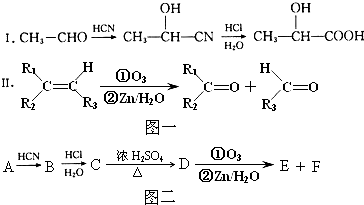
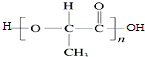 )可以生物降解,请写出以2-丁烯为原料制备聚乳酸的合成路线流程图(无机试剂任选).
)可以生物降解,请写出以2-丁烯为原料制备聚乳酸的合成路线流程图(无机试剂任选).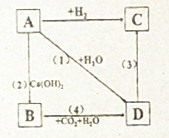 某学生做了一系列有关氯元素单质及其化合物的实验.
某学生做了一系列有关氯元素单质及其化合物的实验.