题目内容
埋在地下的铸铁输油管道,在下列各种情况下,被腐蚀速率最慢的是( )
| A、在潮湿疏松的碱性土壤中 |
| B、在含铁元素较多的酸性土壤中 |
| C、在干燥致密不透气的土壤中 |
| D、在含碳粒较多,潮湿透气的中性土壤中 |
考点:金属的电化学腐蚀与防护
专题:
分析:根据铁生锈的条件进行分析,铁在有水和氧气并存时易生锈,酸和盐能加快铁的锈蚀.
解答:
解:A、在潮湿、疏松、透气的土壤中,铁易生锈;
B、在呈酸性的潮湿土壤中,铁的锈蚀速度很快;
C、在干燥、致密、不透气的土壤中,铁不易生锈;
D、在含碳量较高的潮湿土壤中,铁与水和氧气同时接触,易生锈;
故选C;
B、在呈酸性的潮湿土壤中,铁的锈蚀速度很快;
C、在干燥、致密、不透气的土壤中,铁不易生锈;
D、在含碳量较高的潮湿土壤中,铁与水和氧气同时接触,易生锈;
故选C;
点评:本题考查了铁生锈的条件,完成此题,可以依据已有的知识进行;

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
已知:
(1)Al(OH)3的电离方程式为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-
(2)电解熔融AlCl3不能得到金属铝,AlCl3溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb,
则下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是( )
(1)Al(OH)3的电离方程式为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-
(2)电解熔融AlCl3不能得到金属铝,AlCl3溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb,
则下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是( )
| A、均为强电解质 |
| B、均为弱电解质 |
| C、均为离子化合物 |
| D、均为共价化合物 |
设nA为阿伏加德罗常数,下列说法正确的是( )
| A、常温下,28g C2H4含nA个碳碳双键 |
| B、1 mol Cu和足量稀硝酸反应生成nA NO分子 |
| C、常温常压下,22.4L CCl4含有nA个CCl4分子 |
| D、1mol/L NaCl溶液含有nA个Na+ |
 短周期元素Q、W、X、Y、Z在元素周期表中的相对位置如图所示,其中只有Z为金属元素.则下列说法中,正确的是( )
短周期元素Q、W、X、Y、Z在元素周期表中的相对位置如图所示,其中只有Z为金属元素.则下列说法中,正确的是( )| A、W、X两种元素在自然界中都存在相应的单质 |
| B、Q、Y分别与活泼金属元素形成的化合物中仅含离子键 |
| C、Y、Z分别形成的简单离子中,前者的半径较大 |
| D、X、Z的最高价氧化物对应的水化物之间容易相互发生反应 |
四种短周期元素在周期表中的相对位置如图所示,其中Y为空气中含量最大的元素.下列叙述合理的是( )
| X | Y | |
| Z | W |
| A、元素W位于第三周期第ⅦA族 |
| B、Y、Z都是植物必需的元素 |
| C、原子半径:W>Z>Y>X |
| D、X氧化物的大量排放导致化学烟雾 |
 某有机物与H2按1:1的物质的量之比加成后生成的产物结构为:则该有机物可能的结构有(羟基与碳碳双键相连的结构不稳定,不考虑其存在)( )
某有机物与H2按1:1的物质的量之比加成后生成的产物结构为:则该有机物可能的结构有(羟基与碳碳双键相连的结构不稳定,不考虑其存在)( )| A、4种 | B、5种 | C、6种 | D、7种 |
下列有实验装置的说法,正确的是( )
A、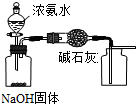 用装置制取干燥纯净的NH3 |
B、 用装置制备Fe(OH)2并能较长时间观察其颜色 |
C、 装置可证明非金属性Cl>C>Si |
D、 装置向左推动针筒活塞可检验该装置的气密性 |

