题目内容
用18.4mol/L的浓H2SO4配制100mL 0.50mol/L的稀H2SO4,请按要求填空( 每 空 1分,共 计 10分)
(1)用量筒量取所需浓H2SO4的体积为 mL;
(2)如果实验室有10mL、20mL、50mL量筒,应选用 mL量筒,实验中还需要用到的仪器有 、 、烧杯、玻璃棒。
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即进行定容
②定容时俯视刻度线
③容量瓶洗净后未干燥 ;
④摇匀后发现液面低于刻度线后加水至溶液的凹液面与刻度线相平 ;
⑤用量筒量取浓H2SO4时仰视刻度线: 。
(4)若定容时液面高于刻度线应采取的措施是 。
(1)2.7ml (2)10mL 100mL 容量瓶 胶头滴管
(3)①偏高 ②偏高 ③无影响 ④偏低 ⑤偏高 (4)重新配制
【解析】
试题分析:(1)溶液在稀释过程中溶质的物质的量不变,所以根据稀释公式可知:C1?V1=C2?V2; V1=(C2?V2) /C1=(100mL×0.50mol/L)÷18.4mol/L=2.7ml;故用量筒量取所需浓H2SO4的体积为2.7ml;(2)为了减小实验误差,应该选择规格合适的量筒来量取浓硫酸,应选用10mL的量筒;由于要配制100ml的溶液,所以实验中还需要用到的仪器有100mL 容量瓶、胶头滴管;(3) ①浓硫酸溶解后未冷至室温即进行定容,当恢复至室温时,溶液的体积偏小,会使溶液的浓度偏高;②定容时俯视刻度线,则溶液的液面低于刻度线,溶液的体积偏小,则所配制的溶液的浓度偏高;③容量瓶洗净后未干燥,由于溶液的体积不变,溶质的物质的量不变,所以溶液的浓度不会产生任何影响;④摇匀后发现液面低于刻度线后加水至溶液的凹液面与刻度线相平,会是溶液的体积偏大,则溶液的浓度就偏低;⑤用量筒量取浓H2SO4时仰视刻度线,则浓硫酸的体积偏多,溶质偏高,会是溶液的浓度偏高;(4)若定容时液面高于刻度线应采取的措施是倒掉溶液,重新配制
考点:考查物质的量浓度的溶液的配制的仪器的选择、使用、误差分析的知识。


 NH
NH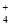 (平衡常数为K1),②Ag++Cl-?
(平衡常数为K1),②Ag++Cl-?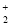 (平衡常数为K3)。
(平衡常数为K3)。