题目内容
【题目】某同学进行下列实验:下列说法合理的是( )
装置 | 操作 | 现象 |
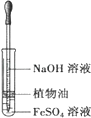
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色 |
A.烧杯A中发生反应:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
B.红棕色气体消失只与NO2和烧杯C中的KI发生反应有关
C.烧杯C中溶液变蓝只与NO2和C中溶液发生反应有关
D.若将铜片换成铁片,则C中的液体也可能变蓝
【答案】D
【解析】解:A.铜与浓硝酸反应生成的是二氧化氮气体,正确的反应为:Cu+4HNO3═Cu(NO3)2+NO2↑+2H2O,故A错误;
B.二氧化氮能够直接与水反应生成硝酸和无色的NO,所以红棕色气体消失与NO2和烧杯C中的KI发生反应有关,也与二氧化氮与水反应有关,故B错误;
C.浓硝酸具有挥发性,则烧杯C中溶液变蓝与NO2和C中溶液发生反应有关,也与挥发出的硝酸有关,故C错误;
D.若将铜片换成铁片,铁与浓硝酸发生钝化,由于浓硝酸具有挥发性,则焕发出的硝酸能够氧化碘离子,导致C中的液体也可能变蓝,故D正确;
故选D.

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
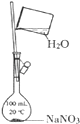
优百分课时互动系列答案【题目】半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g).半水煤气经过下列步骤转化为合成氨的原料.![]()
完成下列填空:
(1)半水煤气含有少量硫化氢.将半水煤气样品通入溶液中(填写试剂名称),出现 , 可以证明有硫化氢存在.
(2)半水煤气在铜催化下实现CO变换:CO+H2O ![]() CO2+H2 , 若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)= .
CO2+H2 , 若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)= .
(3)碱液吸收法是脱除二氧化碳的方法之一.已知:
Na2CO3 | K2CO3 | |
20℃碱液最高浓度(mol/L) | 2.0 | 8.0 |
碱的价格(元/kg) | 1.25 | 9.80 |
若选择Na2CO3碱液作吸收液,其优点是;缺点是 . 如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?写出这种方法涉及的化学反应方程式.
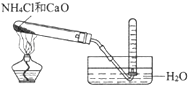
(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案.取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数.
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ、方框中.
②该实验方案中,步骤(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数.