题目内容
4.某二元酸(用H2B表示)在水中的电离方程式是H2B═H++HB-,HB-?H++B2-.在0.1mol/L的Na2B溶液中,下列离子浓度关系式正确的是( )| A. | c(H+)+c(HB-)+2c(H2B)=c(OH-) | B. | c(Na+)+c(OH-)=c(H+)+c(HB-) | ||
| C. | c(Na+)+c(H+)=c(OH-)+c(HB-)+c(B2-) | D. | 2c(B2-)+2c(HB-)=0.2mol/L |
分析 A.H2B第一步完全电离,Na2B溶液中有其电离生成B2-、B2-水解生成的HB-,溶液中不存在H2B;
B.Na2B溶液中有c(Na+)>c(HB-),溶液显碱性:c(OH-)>c(H+),据此进行判断;
C.根据溶液中的电荷守恒判断;
D.根据溶液中的物料守恒分析.
解答 解:A.H2B第一步完全电离,则Na2B溶液中有其电离生成B2-、B2-水解生成的HB-,不存在H2B,故A错误;
B.Na2B溶液中有c(Na+)>c(HB-),溶液显碱性,有c(OH-)>c(H+),则c(Na+)+c(OH-)>c(HB-)+c(H+),c(Na+)+c(OH-)=c(HB-)+c(H+)不成立,故B错误;
C.溶液中电荷守恒式为:c(Na+)+c(H+)=c(HB-)+2c(B2-)+c(OH-),故C错误;
D.由物料守恒式可得:c(Na+)=2c(HB-)+2c(B2-)=0.02mol/L,故D正确;
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,正确分析题干信息为解答关键,注意掌握物料守恒、电荷守恒及盐的水解原理的含义及应用方法,试题培养了学生的灵活应用能力.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
12.将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g),不能判断该分解反应已经达到化学平衡的是( )
| A. | v(NH3)正=2v(CO2)逆 | B. | 密闭容器中总压强不变 | ||
| C. | 密闭容器中氨气的体积分数不变 | D. | 密闭容器中混合气体的密度不变 |
19.电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
| A. | 阳极反应为Fe-2e-═Fe2+ | |
| B. | 电路中每转移12mol电子,最多有1molCr2O${\;}_{7}^{2-}$被还原 | |
| C. | 过程中有Fe(OH)3沉淀生成 | |
| D. | 电解过程中溶液pH不会变化 |
9.现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复).
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物
(1)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-).
(2)写出E溶液与过量的B溶液反应的离子方程式2Al3++3SO42-+3Ba2++8OH-=2AlO2-+3BaSO4↓+4H2O.
(3)已知:NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l);△H=-a kJ•mol-1.请写出B与C的稀溶液反应的热化学方程式OH-(aq)+H+(aq)=H2O(1)△H=-akJ/mol.
(4)在100 mL 0.1 mol•L-1E溶液中,逐滴加入35 mL 2 mol•L-1NaOH溶液,最终得到沉淀的物质的量为0.01mol.
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3、SO42- |
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物
(1)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-).
(2)写出E溶液与过量的B溶液反应的离子方程式2Al3++3SO42-+3Ba2++8OH-=2AlO2-+3BaSO4↓+4H2O.
(3)已知:NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l);△H=-a kJ•mol-1.请写出B与C的稀溶液反应的热化学方程式OH-(aq)+H+(aq)=H2O(1)△H=-akJ/mol.
(4)在100 mL 0.1 mol•L-1E溶液中,逐滴加入35 mL 2 mol•L-1NaOH溶液,最终得到沉淀的物质的量为0.01mol.
13.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
| B | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结. | NH4Cl固体可以升华 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| A. | A | B. | B | C. | C | D. | D |
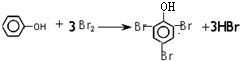 .
. ;
; +
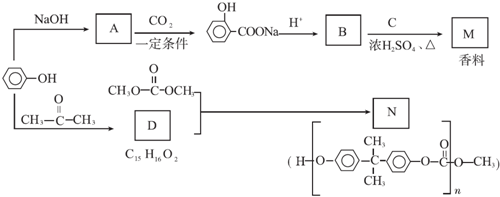
+ $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$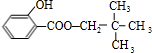 +H2O.
+H2O.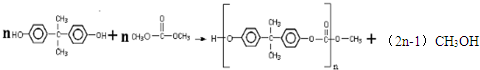 ,反应类型为缩聚反应.
,反应类型为缩聚反应.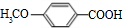 .
.