题目内容
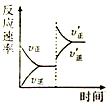 一定条件下,在某密闭容器中进行如下反应:mA(g)+nB(g)?pC(g)+qD(s),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
一定条件下,在某密闭容器中进行如下反应:mA(g)+nB(g)?pC(g)+qD(s),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )| A、正反应是放热反应 |
| B、逆反应是放热反应 |
| C、m+n<p+q |
| D、m+n>p+q |
考点:化学平衡的影响因素,化学反应速率变化曲线及其应用
专题:化学平衡专题
分析:若增大压强或升高温度,依据图象分析可知,逆反应速率小于正反应速率,说明平衡向正反应方向移动,依据平衡移动原理分析判断.
解答:
解:若增大压强或升高温度,依据图象分析可知,逆反应速率小于正反应速率,说明平衡向正反应方向移动,增大压强平衡正向移动,说明m+n>p+q,升温平衡正向移动,说明正反应吸热,则逆反应放热,所以B正确,A、C、D错误,
故选B.
故选B.
点评:本题考查化学反应速率与化学平衡的图象问题,题目难度不大,注意压强和温度对化学平衡的影响分析,掌握基础是关键.

练习册系列答案
相关题目
某有机物结构简式如图,下列有关它的说法正确的是( )
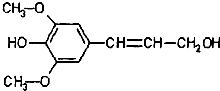

| A、分子式是C11H14O4,属于芳香烃 |
| B、分子中所有碳原子不可能在同一平面 |
| C、不能与Na反应放出H2 |
| D、能发生的反应类型有氧化、取代、加成 |
氢氰酸(HCN)的下列性质中,不可以证明它是弱电解质的是( )
| A、常温下,0.01mol/L氢氰酸溶液的pH大于2 |
| B、HCN溶液用水稀释后,氢离子浓度下降 |
| C、NaCN溶液呈碱性 |
| D、相同条件下,0.01mol/L氢氰酸溶液的导电性比0.01 mol/L 氯化氢溶液的差 |
为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,再向过滤中加入适量的盐酸,这种试剂是( )
| A、NH3.H2O |
| B、NaOH |
| C、Na2CO3 |
| D、MgCO3 |
在室温下,等体积的酸和碱的溶液,混合后pH一定等于7的是( )
| A、同浓度的H2SO4溶液于KOH溶液 |
| B、pH=3的盐酸和pH=11的氨水 |
| C、pH=3的硫酸和pH=11的KOH |
| D、pH=3的醋酸和pH=11的KOH溶液 |
根据化学常识,下列说法正确的是( )
| A、施用碳铵(NH4HCO3)后应立即盖上土壤 |
| B、复合肥是两种或两种以上化肥的混合物 |
| C、可用工业用盐作食盐用于烹调 |
| D、三聚氰胺(C3N6H6)俗称“蛋白精”,加入到奶粉中,可提高蛋白质的含量 |
以下表述不符合元素周期律观点的是( )
| A、酸性:H3PO4>HNO3>HClO4 |
| B、稳定性:HF>H2O>NH3 |
| C、微粒半径:F->Na+>Mg2+ |
| D、碱性:KOH>NaOH>Mg(OH)2 |
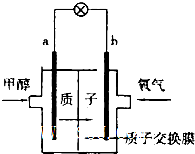 某研究性学习小组为了证明某酸HmA是强酸还是弱酸,设计了如下实验方案,请回答有关问题:
某研究性学习小组为了证明某酸HmA是强酸还是弱酸,设计了如下实验方案,请回答有关问题: