题目内容
17.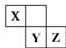 X、Y、Z 三种短周期元素在周期表中的位置如右图,X 通过共用三对电子形成 X2分子,下列说法不正确的是( )
X、Y、Z 三种短周期元素在周期表中的位置如右图,X 通过共用三对电子形成 X2分子,下列说法不正确的是( )| A. | 化合物 XZ3 中各原子均满足 8 电子的稳定结构 | |
| B. | X、Y、Z 三种元素形成的含氧酸都是强酸 | |
| C. | 常温下,Z 单质可与 Y 的氢化物发生置换反应 | |
| D. | 一定条件下,X2与Al反应得到 AlX |
分析 由X、Y、Z 三种短周期元素在周期表中的位置,X 通过共用三对电子形成 X2分子,可知X为N,Y为S,Z为Cl,
A.NCl3 中N原子的3个单电子分别与氯原子提供的单电子形成共用电子对;
B.亚硝酸、亚硫酸、HClO等均为弱酸;
C.氯气与硫化氢反应生成HCl、S;
D.氮气与Al可反应生成原子晶体AlN.
解答 解:由X、Y、Z 三种短周期元素在周期表中的位置,X 通过共用三对电子形成 X2分子,可知X为N,Y为S,Z为Cl,
A.NCl3 中N原子的3个单电子分别与氯原子提供的单电子形成共用电子对,则各原子均满足 8 电子的稳定结构,故A正确;
B.亚硝酸、亚硫酸、HClO等均为弱酸,最高价含氧酸均为强酸,故B错误;
C.氯气与硫化氢反应生成HCl、S,为置换反应,故C正确;
D.一定条件下,氮气与Al发生氧化还原反应生成原子晶体AlN,故D正确;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、分子及原子结构、元素化合物为解答本题的关键,侧重分析与应用能力的考查,注意选项D为解答的难点,题目难度不大.

练习册系列答案
相关题目
8.下列化学方程式中,能用离子方程式 H++OH-=H2O 表示的是( )
| A. | H2SO4+Ba(OH)2=BaSO4↓+2H2O | B. | HCl+NaOH=NaCl+H2O | ||
| C. | NaOH+CH3COOH=CH3COONa+H2O | D. | Cu(OH)2+2HCl=CuCl2+2H2O |
5.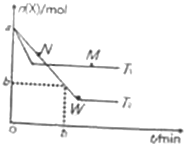 在2L密闭容器中通入amolX气体并发生反应:2X(g)?Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示.下列叙述不正确的是( )
在2L密闭容器中通入amolX气体并发生反应:2X(g)?Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示.下列叙述不正确的是( )
 在2L密闭容器中通入amolX气体并发生反应:2X(g)?Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示.下列叙述不正确的是( )
在2L密闭容器中通入amolX气体并发生反应:2X(g)?Y(g),在T1、T2温度下,X的物质的量n(X)随时间t变化的曲线如图所示.下列叙述不正确的是( )| A. | 正反应方向为放热反应 | |
| B. | 在T2温度下,在0~t1时间内,v(Y)=$\frac{a-b}{{t}_{1}}$mol•(L•min)-1 | |
| C. | M点的正反应速率v(正)大于N点的逆反应速率v(逆) | |
| D. | W点时再加入一定量X,平衡后X的转化率增大 |
12.下列有关物质分类或归类正确的是( )
①混合物:盐酸、漂白粉、水玻璃、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、石膏、冰醋酸、石炭酸
④同素异形体:C60、C70、金刚石、石墨烯
⑤同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑥同分异构体:乙二酸二乙酯、乙二酸乙二酯、二乙酸乙二酯.
①混合物:盐酸、漂白粉、水玻璃、水银
②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、石膏、冰醋酸、石炭酸
④同素异形体:C60、C70、金刚石、石墨烯
⑤同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑥同分异构体:乙二酸二乙酯、乙二酸乙二酯、二乙酸乙二酯.
| A. | ①③④ | B. | ②③④ | C. | ③④ | D. | ②④⑥ |
2.下列各组粒子属于同位素的是( )
| A. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | B. | ${\;}_{19}^{40}$ K 和${\;}_{20}^{40}$ Ca | ||
| C. | O2 和 O3 | D. | H2O 和 D2O |
9.化学反应 A2+B2═2AB 的能量变化如图所示,则下列说法中正确的是( )
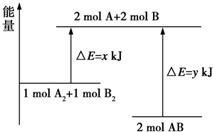

| A. | 该反应过程吸收能量 | |
| B. | 断裂 1molA-A 键和 1molB-B 键可放出 x kJ 能量 | |
| C. | 形成 2molA-B 键需要放出 y kJ 能量 | |
| D. | 2molAB 的总能量高于 1molA2和 1molB2的总能量 |
6.下列物质中,属于酚类的是( )
| A. | C6H5CH2OH | B. | 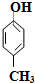 | C. | 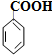 | D. | CH3Cl |
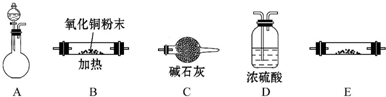
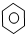 ③CH3CH2Cl ④CH3COOH ⑤聚乙烯五种物质中:
③CH3CH2Cl ④CH3COOH ⑤聚乙烯五种物质中: