题目内容
6.设NA为阿伏加德罗常数,以下叙述正确的是( )| A. | 1 L 0.1 mol/L NH4NO3溶液中含有铵根离子数目为0.1NA | |
| B. | 标准状况下,22.4 L SO3中含有的氧原子数为3NA | |
| C. | 标准状况下,22.4L氯气与含有1 mol FeI2的溶液反应时,转移的电子数为2NA | |
| D. | 常温常压下,16g O2作氧化剂时转移电子数一定为2NA |
分析 A、铵根离子水解导致铵根离子小于0.1mol;
B、三氧化硫是固体;
C、标准状况下,22.4L氯气的物质的量为1mol,与有1 mol FeI2的溶液反应时,碘化亚铁过量,氯气完全反应;
D、根据氧元素的价态有-1价和-2价来分析.
解答 解:A、铵根离子水解导致铵根离子小于0.1mol,所以铵根离子的个数小于0.1NA,故A错误;
B、三氧化硫是固体,气体摩尔体积不适用,故B错误;
C、标准状况下,22.4L氯气的物质的量为1mol,与有1 mol FeI2的溶液反应时,碘化亚铁过量,氯气完全反应,所以1mol氯气转移电子数为2NA,故C正确;
D、氧元素的价态有-1价和-2价,1molO2作氧化剂后如果被还原为-1价,则转移2mol电子,若被还原为-2价,则转移4mol电子,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握物质的性质和氧化还原反应电子的转移.

练习册系列答案
相关题目
17.醋酸镍[(CH3COO)2Ni]是一种重要的化工原料.一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料制取醋酸镍的工艺流程图如图1:

相关离子生成氢氧化物的pH和相关物质的溶解性如表:
(1)NH4F的电子式为
(2)将含镍原料粉碎的目的是提高镍的浸出率
(3)调节pH步骤中,溶液pH的调节范围是5.0≤pH<6.7.
(4)滤渣1和滤渣3主要成分的化学式分别是SiO2、CaSO4、CaF2.
(5)写出氧化步骤中加入H2O2发生反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O.
(6)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体.写出该反应的化学方程式:NiS+H2SO4+2HNO3═NiSO4+SO2↑+2NO↑+2H2O.
(7)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图2.酸浸的最佳温度与时间分别为70℃、120min.
(8)沉镍过程中,若c(Ni2+)=2.0mol•L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol•L-1],则需要加入Na2CO3固体的质量最少为31.8g.(保留小数点后1位有效数字).

相关离子生成氢氧化物的pH和相关物质的溶解性如表:
| 金属离子 | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
| 物质 | 20℃时溶解性(H2O) |
| CaSO4 | 微溶 |
| NiF | 可溶 |
| CaF | 难溶 |
| NiCO3 | Ksp=1.0×10-6 |

(2)将含镍原料粉碎的目的是提高镍的浸出率
(3)调节pH步骤中,溶液pH的调节范围是5.0≤pH<6.7.
(4)滤渣1和滤渣3主要成分的化学式分别是SiO2、CaSO4、CaF2.
(5)写出氧化步骤中加入H2O2发生反应的离子方程式2Fe2++H2O2+2H+═2Fe3++2H2O.
(6)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体.写出该反应的化学方程式:NiS+H2SO4+2HNO3═NiSO4+SO2↑+2NO↑+2H2O.
(7)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图2.酸浸的最佳温度与时间分别为70℃、120min.
(8)沉镍过程中,若c(Ni2+)=2.0mol•L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5mol•L-1],则需要加入Na2CO3固体的质量最少为31.8g.(保留小数点后1位有效数字).
14.根据下列实验操作和现象所得结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 溴乙烷与NaOH乙醇溶液共热产生的气体通入KMnO4酸性溶液中,溶液褪色 | 产生的气体为乙烯 |
| B | 向浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液中滴加NaOH溶液,出现红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
| C | 取少量淀粉水解液于试管中,加入过量氢氧化钠溶液和新制Cu(OH)2悬浊液,加热至沸腾,出现砖红色沉淀 | 淀粉已完全水解 |
| D | 在CuSO4溶液中加入KI溶液,再加入苯,振荡,有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为CuI |
| A. | A | B. | B | C. | C | D. | D |
1.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 在50g质量分数为46%的乙醇水溶液中,含有氢原子数为3NA | |
| B. | 80℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | lmol有机物CH3-CH=CH-CH2-CH3中最多有9NA个原子在同一平面上 | |
| D. | l04g苯乙烯(C6H5-CH=CH2)中含有8NA的碳氢键和4NA的碳碳双键 |
11.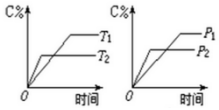 可逆反应m A(s)+n B(g)?e C(g)+f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
可逆反应m A(s)+n B(g)?e C(g)+f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
 可逆反应m A(s)+n B(g)?e C(g)+f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
可逆反应m A(s)+n B(g)?e C(g)+f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )| A. | 达平衡后,若升温,则K减小 | |
| B. | 达平衡后,加入催化剂C%增大 | |
| C. | 化学方程式中n>e+f | |
| D. | 达平衡后,若增加A的量,B的转化率增大 |
18.巨噬细胞控制肌肉再生的“分子开关”的结构如图所示.下列有关说法错误的是( )
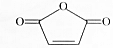

| A. | 分子式为C4H2O3 | B. | 能发生水解反应 | ||
| C. | 一氯代物有2种 | D. | 能使酸性KMnO4溶液褪色 |
15.在密闭容器中,反应2X(g)+Y(g)?3Z(g)达到平衡后,若将容器体积缩小一半,对反应产生的影响是( )
| A. | v(正)减小,v(逆)增大 | B. | v(正)增大,v(逆)减小 | C. | v(正)、v(逆)都减小 | D. | v(正)、v(逆)都增大 |
6.已知碘在四氯化碳液体中的溶解度远大于在水中的溶解度,且固体碘在受热时,易直接变成气体,欲把碘从饱和碘水中分离出来,可采用的方法和主要仪器为( )
| A. | 蒸发、结晶与蒸发皿 | B. | 过滤与漏斗 | ||
| C. | 萃取、分液与分液漏斗 | D. | 蒸馏与蒸馏装置 |