题目内容
18.三氯化锑(SbCl3)是锑元素的一种氯化物,常温常压下为无色固体.Ⅰ.经查阅资料得知:无水SbCl3在空气中易潮解,加热易升华.某研究性学习小组设计了制备无水SbCl3的实验方案,装置示意图(夹持装置略去)及操作步骤如下:
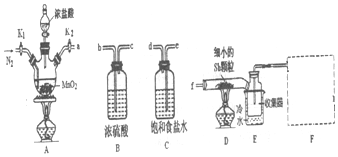
(1)按照实验要求组装仪器.接口连接顺序为:a接e、d接b、c接f.
(2)装置A中反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)装置E中冷水浴的作用为使SbCl3变为固体.
(4)实验开始时,先点燃A处酒精灯(选填“A”或“D”).
(5)体系冷却后,停止通入Cl2,接下来的一步操作及理由是通入氮气,以排出装置内的氯气,避免污染空气.
(6)在F虚线框中画出所必须的装置并注明试剂.
(7)该实验方案制得的SbCl3中可能存在的杂质是Sb2O3.
Ⅱ.(1)实验室可利用的SbCl3水解反应制取Sb2O3、SbCl3的水解分三步进行,中间产物有SbOCl等.其总反应可表示为2SbCl3+3H2O=Sb2O3+6HCl.
(2)为了得到较多、较纯Sb2O3,操作时要将SbCl3徐徐加入大量水中,反应后期还要加入少量氨水.从平衡移动的角度说明这两项操作的作用是加入少量氨水,可使生成物浓度降低,平衡正向移动,且反应生成HCl,加入氨气,发生中和反应,平衡正向移动.
分析 Ⅰ.A用于制备氯气,然后分别经过C、B,分别除去HCl、水,在D中与Sb反应生成SbCl3,因SbCl3加热易升华,收集装置E应在较低温度下,F为尾气处理装置,且防止空气中水蒸气进入E,应用碱石灰,体系冷却后,停止通入Cl2,且通入氮气,以排出装置内氯气;
Ⅱ.SbCl3水解反应制取Sb2O3,同时生成HCl,水解反应为可逆反应,加入碱,有利于平衡正向移动,以此解答该题.
解答 解:Ⅰ.(1)由以上分析可知连接顺序为a→e;d→c;b→f,故答案为:e;d;b;c;
(2)装置A用于制备氯气,反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(3)因无水SbCl3在空气中易潮解,加热易升华,则装置E中冷水浴的作用为使SbCl3变为固体,故答案为:使SbCl3变为固体;
(4)实验室应先通入氯气,使装置内空气排出,利于氯气和锑的反应,故答案为:A;
(5)体系冷却后,停止通入Cl2,接下来的一步操作是通入氮气,以排出装置内的氯气,避免污染空气,
故答案为:通入氮气,以排出装置内的氯气,避免污染空气;
(6)F为尾气处理装置,且防止空气中水蒸气进入E,应用碱石灰,装置为 ,故答案为:
,故答案为: ;
;
(7)SbCl3易分解,可水解生成Sb2O3,则可能含有Sb2O3杂质,故答案为:Sb2O3;
Ⅱ.(1)SbCl3水解反应制取Sb2O3,同时生成HCl,方程式为2SbCl3+3H2O=Sb2O3+6HCl,故答案为:2SbCl3+3H2O=Sb2O3+6HCl;
(2)操作时要将SbCl3徐徐加入大量水中,反应后期还要加入少量氨水,可使生成物浓度降低,平衡正向移动,且反应生成HCl,加入氨气,发生中和反应,平衡正向移动,利于生成Sb2O3,故答案为:加入少量氨水,可使生成物浓度降低,平衡正向移动,且反应生成HCl,加入氨气,发生中和反应,平衡正向移动.
点评 本题考查物质制备的实验操作和实验设计,为高考常见题型和高频考点,题目难度中等,侧重考查元素化合物的性质应用、实验基本操作的分析判断、实验现象的推断和应用,试题综合性较强,有利于培养学生灵活应用基础知识的能力.

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl- 等,其中HClO2和ClO2都具有漂白作用.已知POH=-lgc(OH-),经测定25℃时各组分含量随POH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )
亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl- 等,其中HClO2和ClO2都具有漂白作用.已知POH=-lgc(OH-),经测定25℃时各组分含量随POH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )| A. | 亚氯酸钠在碱性条件下较稳定 | |
| B. | PH=7时,溶液中含氯微粒的浓度大小:c(ClO2-)>c(HClO2)>c (ClO2) | |
| C. | HClO2的电离平衡常数的数值Ka=10-6 | |
| D. | 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有2c(HClO2)+c(H+)=2c(ClO2-)+c(OH-) |
Ⅰ.某研究小组将纯净的SO2气体通入0.5mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀.为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一:
①请在下表空白处填写相关实验现象
| 实 验 步 骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的10mL 0.5mol/L BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体. | 无现象 | 假设一成立 |
| 实验2:在盛有不含O2的10mL 0.5mol/L Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体. | 白色沉淀生成 |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲.实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2NO3-+2H2O=3SO42-+2NO↑+4H+.
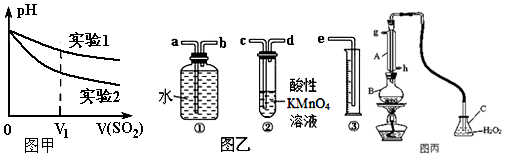
Ⅱ.我国规定空气中SO2含量不得超过0.02mg/L.某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量.
(1)若原料气从左向右流,上述装置连接的顺序是:原料气→c→d→b→a→e(用字母和箭头表示).当装置②中出现溶液紫(或紫红)色褪去现象时,立即停止通气.
(2)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是B.
A.NaOH溶液 B.溴水C.氨水 D.BaCl2溶液
Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L.某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定.
(1)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为0.192g/L.
(2)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施盐酸易挥发,用不挥发的强酸例如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,排除盐酸挥发的影响.
 电解质溶液的电导率越大,导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度 均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温 Ksp[(CH3)2NH•H2O3=1.6×l04),利用传感器测得滴定过程中溶液的电导率如图所示》下列说法正确的是( )
电解质溶液的电导率越大,导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度 均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温 Ksp[(CH3)2NH•H2O3=1.6×l04),利用传感器测得滴定过程中溶液的电导率如图所示》下列说法正确的是( )| A. | b、c、d三点的溶液中水的电离程度:b<d<c | |
| B. | a 点溶液中:c(Na+)=2c(OH-)-2c(H+) | |
| C. | d 点溶液中:c[(CH3)2NH2+]+c(H+)-(OH-)=0.100mol•L-1 | |
| D. | e 点溶液中:c(H+)>c[(CH3)2NH2+]+2c[(CH3)2NH•H2O] |
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
| A. | 通过测定大米浸泡液的pH检验大米新鲜度 | |
| B. | 用含Fe2+的检测试剂检验自来水中余氯的含量 | |
| C. | 向食盐样品中加还原剂和淀粉检测食盐的含碘量 | |
| D. | 通过观察放入检测液中鸡蛋的沉浮检验鸡蛋新鲜度 |
化学在生活中有着广泛的应用,下列对应关系错误的是( )
化学性质 | 实际应用 | |
A. | 三价铁比二价铜氧化性强 | FeCl3腐蚀Cu |
B. | 次氯酸盐具有氧化性 | 次氯酸钙可做漂白剂 |
C. | 稀硝酸可与银反应 | 稀硝酸可除去试管内壁 |
D. | HF能与Si反应 | 氢氟酸在玻璃器皿上刻蚀标记 |

 ;F含有的官能团名称是羧基、羟基.
;F含有的官能团名称是羧基、羟基. .
. 或
或 .
.
 刻制印刷电路板
刻制印刷电路板