题目内容
下列有关反应的反应类型叙述正确的是( )
| A、HClO+NaOH=NaClO+H2O 非氧化还原反应 复分解反应 |
| B、MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O氧化还原反应 分解反应 |
| C、3Fe+2O2=Fe3O4 非氧化还原反应 化合反应 |
| D、Fe2O3+3CO=2Fe+3CO2 氧化还原反应 置换反应 |
考点:氧化还原反应,化学基本反应类型
专题:
分析:含元素化合价变化为氧化还原反应,结合四种基本反应类型来解答.
解答:
解:A.没有元素的化合价变化,为非氧化还原反应,为酸、碱的中和反应,属于复分解反应,故A正确;
B.Mn、Cl元素的化合价变化,为氧化还原反应,反应物有两种,不属于分解反应,故B错误;
C.Fe、O元素的化合价变化,为氧化还原反应,故C错误;
D.Fe、C元素的化合价变化,为氧化还原反应,反应物中没有单质,不属于置换反应,故D错误;
故选A.
B.Mn、Cl元素的化合价变化,为氧化还原反应,反应物有两种,不属于分解反应,故B错误;
C.Fe、O元素的化合价变化,为氧化还原反应,故C错误;
D.Fe、C元素的化合价变化,为氧化还原反应,反应物中没有单质,不属于置换反应,故D错误;
故选A.
点评:本题考查氧化还原反应及四种基本反应类型,为高频考点,把握反应中元素的化合价变化及物质的类别及反应分类为解答的关键,侧重反应类型判断的考查,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列说法正确的是( )
A、 装置用于Cu和浓H2SO4制取少量的SO2气体 |
B、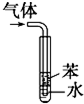 用于吸收HCl气体能防倒吸 |
C、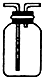 可用于收集气体H2、CO2、Cl2、NH3 |
D、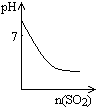 表示将SO2气体通入溴水中,所得溶液的pH变化 |
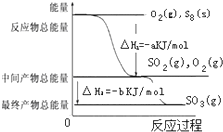 在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的△H表示生成1 mol含硫产物的数据).由图得出的结论正确的是( )
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的△H表示生成1 mol含硫产物的数据).由图得出的结论正确的是( )| A、S8(s)的燃烧热△H=-8akJ?mol-1 |
| B、2SO3(g)?2SO2(g)+O2(g);△H=-2b kJ?mol-1 |
| C、S8(s)+8O2(g)=8SO2(g);△H=-a kJ?mol-1 |
| D、由1molS8(s)生成SO3(g)的反应热△H=-(a+b)kJ?mol-1 |
一定条件下,反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在5L密闭容器中进行,10s后H2O的物质的量增加了0.60mol,则10s内反应的速率v(X)可表示为( )
| A、v (NH3)=0.008 mol/(L?s) |
| B、v (NO)=0.04 mol/(L?s) |
| C、v (O2)=0.006 mol/(L?s) |
| D、v (H2O)=0.06 mol/(L.min) |
不属于新能源的是( )
| A、风能 | B、潮汐能 |
| C、乙醇汽油 | D、生物质能 |
如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )
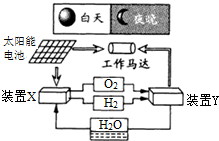

| A、该系统中只存在3种形式的能量转化 |
| B、装置Y中电能转化为化学能 |
| C、装置X能实现燃料电池的燃料和氧化剂再生 |
| D、装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
已知在101kPa、25℃条件下,2mol氢气完全燃烧生成水蒸气放出484kJ的热量,下列热化学方程式正确的是( )
A、H2O(g)=H2 (g)+
| ||
| B、2H2 (g)+O2(g)=2H2O(l)△H=-484 kJ∕mol | ||
C、H2 (g)+
| ||
| D、2H2 (g)+O2(g)=2H2O(g)△H=+484 kJ∕mol |
溶液、胶体、浊液这三种分散系的本质区别是( )
| A、分散质粒子大小不同 |
| B、稳定性不同 |
| C、是否具有丁达尔效应 |
| D、能否透过滤纸 |