题目内容
1.与OH-有相同电子数和质子数的粒子是( )| A. | F- | B. | Cl- | C. | NH3 | D. | H2O |
分析 根据微粒中质子数为各原子的质子数之和,若微粒为分子,质子数=电子数;若微粒为阳离子,电子数=质子数-电荷数;若微粒为阴离子,电子数=质子数+电荷数,据此分析.
解答 解:OH-的质子数为9,电子数为10;
A.F-中质子数为9,电子数=9+1=10,故A正确;
B.Cl-中质子数为17,电子数=17+1=18,故B错误;
C.NH3中质子数=电子数=10,故C错误;
D.H2O中质子数为10,电子数=质子数=10,故D错误;
故选:A.
点评 本题考查了微粒中质子数和电子数之间的关系,难度不大,明确阳离子中电子数=质子数-电荷数、阴离子中电子数=质子数+电荷数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列说法中,正确的是( )
| A. | 石油裂化的目的是获得更多的乙烯,丙烯等原料 | |
| B. | 石油分馏,煤的干馏发生的都是物理变化 | |
| C. | 油脂的皂化发生的是化学变化 | |
| D. | 向蛋白质溶液中分别加入硫酸铜,硫酸铵的浓溶液都可以发生盐析 |
9.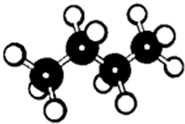 如图是一个分子的球棍模型图,图中大小“球”表示两种元素的原子,“棍”表示化学键.该模型表示的有机物是( )
如图是一个分子的球棍模型图,图中大小“球”表示两种元素的原子,“棍”表示化学键.该模型表示的有机物是( )
 如图是一个分子的球棍模型图,图中大小“球”表示两种元素的原子,“棍”表示化学键.该模型表示的有机物是( )
如图是一个分子的球棍模型图,图中大小“球”表示两种元素的原子,“棍”表示化学键.该模型表示的有机物是( )| A. | 正丁烷 | B. | 正丁烯 | C. | 异丁烷 | D. | 苯 |
16.含有单官能团分子式为C5H10O2且不能与饱和NaHCO3溶液反应的有机物有(不含立体异构)( )
| A. | 6种 | B. | 7种 | C. | 9种 | D. | 9种以上 |
6.下列说法不正确的是( )
| A. | 已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键 | |
| B. | 对于CaCO3(s)═CaO(s)+CO2(g) 任何温度下都不能自发进行 | |
| C. | 实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键 | |
| D. | 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),△H=+489.0 kJ/mol. CO(g)+$\frac{1}{2}$O2(g)═CO2(g),△H=-283.0 kJ/mol. C(石墨)+O2(g)═CO2(g),△H=-393.5 kJ/mol. 则4Fe(s)+3O2(g)═2Fe2O3(s),△H=-1641.0 kJ/mol |
10.生活中的一些小常识往往包含化学知识,以下叙述不正确的是( )
| A. | 用热的纯碱水洗涤油污 | |
| B. | 用食醋消除暖水瓶中的水垢 | |
| C. | 用碘水来检测成熟的苹果中是否含有淀粉 | |
| D. | 纤维素在人体内可水解为葡萄糖,故可作为人类的营养物质 |

 .
. .
.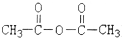 )反应制得.
)反应制得.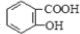 ;
;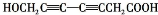 、
、 .
.