题目内容
6.用NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 1mol乙烯分子中含有共用电子对数为6NA | |
| B. | 常温常压下,32gO2、O3的混合物含有Na个氧原子 | |
| C. | 标准状况下,2.24 L CH2Cl2含有的分子数等于0.1 NA | |
| D. | 7.1 g C12与足量NaOH溶液反应转移0.2×6.02×1023个电子 |
分析 A、乙烯中含6对共用电子对;
B、氧气和臭氧均由氧原子构成;
C、标况下二氯甲烷为液体;
D、求出氯气的物质的量,然后根据1mol氯气和氢氧化钠反应时转移1mol电子来分析.
解答 解:A、乙烯中含6对共用电子对,故1mol乙烯中含6NA对共用电子对,故A正确;
B、氧气和臭氧均由氧原子构成,故32g氧气和臭氧的混合物中含有的氧原子的物质的量为n=$\frac{32g}{16g/mol}$=2mol,故含2NA个氧原子,故B错误;
C、标况下二氯甲烷为液体,故不能根据气体摩尔体积来计算其物质的量和含有的分子个数,故C错误;
D、7.1g氯气的物质的量为0.1mol,而氯气和氢氧化钠的反应为:Cl2+2NaOH=NaCl+NaClO+H2O,1mol氯气和氢氧化钠反应时转移1mol电子,故0.1mol氯气和氢氧化钠反应转移0.1NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
16.糖类、脂肪和蛋白质是人体必需的三大营养物质.以下叙述中,不正确的是( )
| A. | 植物油能使溴的四氯化碳溶液褪色 | B. | 淀粉水解的最终产物是葡萄糖 | ||
| C. | 葡萄糖能发生水解反应 | D. | 含有苯环的蛋白质遇浓硝酸变黄色 |
17.下列物质中不属于油脂的是( )
①花生油②润滑油③甘油④棉籽油⑤牛油⑥汽油.
①花生油②润滑油③甘油④棉籽油⑤牛油⑥汽油.
| A. | ①② | B. | ②③⑥ | C. | ③④ | D. | ②⑤⑥ |
14.下列说法正确的是( )
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 鸡蛋清溶液中加入饱和硫酸钠溶液,生成的沉淀物不能再溶解 | |
| C. | 酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色会褪去 | |
| D. | 维生素C( 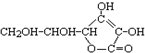 )溶液中滴加KI淀粉溶液,立即变蓝色 )溶液中滴加KI淀粉溶液,立即变蓝色 |
1.下列除去杂质(括号内为杂质)的方法正确的是( )
①乙烷(乙烯)催化剂、加热条件下通入氢气
②乙酸乙酯(乙酸)用饱和碳酸钠溶液洗涤、分液
③苯(乙酸)用氢氧化钠溶液洗涤、分液
④乙醇(乙酸)加足量生石灰、蒸馏
⑤苯(苯酚)加入浓溴水、过滤.
①乙烷(乙烯)催化剂、加热条件下通入氢气
②乙酸乙酯(乙酸)用饱和碳酸钠溶液洗涤、分液
③苯(乙酸)用氢氧化钠溶液洗涤、分液
④乙醇(乙酸)加足量生石灰、蒸馏
⑤苯(苯酚)加入浓溴水、过滤.
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ②④⑤ |
11.下列叙述中正确的是( )
| A. | 标准状况下,40gSO3的体积约为11.2L | |
| B. | 硫粉在过量的纯氧中燃烧生成SO3 | |
| C. | 使用清洁能源是防止酸雨发生的重要措施之一 | |
| D. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
18.Na2O2、HClO、SO2、O3都具有漂白性.下列说法不正确的是( )
| A. | 过氧化钠、二氧化硫属于氧化物,而次氯酸属于弱酸,臭氧属于单质 | |
| B. | 它们都能使品红溶液褪色,但褪色原理不同;加热褪色的溶液都能变红 | |
| C. | 二氧化硫能与其他三种物质发生氧化还原反应,二氧化硫表现还原性 | |
| D. | 过氧化钠溶于水产生的气体与臭氧互为同素异形体,臭氧比氧气活泼 |
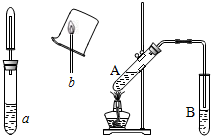 乙醇性质探究
乙醇性质探究