题目内容
二元酸H2A在水中发生电离:H2A══H ++HA -和HA -A. NaHA: c(Na +)>c(HA -)>c(OH -)>c(H +)?
B. NaHA: c(Na +)=c(A 2-)+c(HA -)?
C.Na2A: c(Na +)>c(A 2-)>c(OH -)>c(H +)?
D.H2A: c(H +)=c(HA -)+2c(A 2-)+c(OH -)
A?
解析:由电离方程式看出,该酸第一步完全电离,第二步为可逆电离,在NaHA溶液中应为?c(H +)>c(OH -),故A不正确。由物料守恒c(Na +)=c(A 2-)+c(HA -),C中Na2A溶液由于A 2-水解而使溶液呈碱性,则c(Na +)>c(A 2-)>c(OH -)>c(H +),D中由电荷守恒可知正确。

练习册系列答案
相关题目
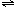 H++A2-,则下列几种物质的水溶液中关系式不正确的是
H++A2-,则下列几种物质的水溶液中关系式不正确的是