题目内容
 三种短周期A、B、C在元素周期表中的位置如图所示.已知A、B、C 三种元素的原子最外层电子数之和为12.据此填空:
三种短周期A、B、C在元素周期表中的位置如图所示.已知A、B、C 三种元素的原子最外层电子数之和为12.据此填空:(1)C的氢化物的结构式为
(2)A的元素符号为
(3)B的最高价氧化物的分子式为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期A、B、C在元素周期表中的位置可知,A、C处于第二周期、B处于第三周期,设A原子的最外层电子数为x,则B原子最外层电子数为x+1,C的原子最外层电子数为x+2,又A、B、C 三种元素的原子最外层电子数之和为12,则有x+x+1+x+2=12,解得x=3,所以A为B元素,B为Si元素,C为N元素,据此解答.
解答:
解:由短周期A、B、C在元素周期表中的位置可知,A、C处于第二周期、B处于第三周期,设A原子的最外层电子数为x,则B原子最外层电子数为x+1,C的原子最外层电子数为x+2,又A、B、C 三种元素的原子最外层电子数之和为12,则有x+x+1+x+2=12,解得x=3,所以A为B元素,B为Si元素,C为N元素,
(1)C的氢化物为NH3,结构式为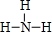 ,故答案为:
,故答案为: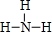 ;
;
(2)由上述分析可知,A的元素符号为B,在元素周期表中位于第二周期ⅢA族,故答案为:B;二、ⅢA;
(3)B为Si元素,其最高价氧化物的分子式为SiO2,故答案为:SiO2.
(1)C的氢化物为NH3,结构式为
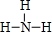 ,故答案为:
,故答案为: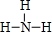 ;
;(2)由上述分析可知,A的元素符号为B,在元素周期表中位于第二周期ⅢA族,故答案为:B;二、ⅢA;
(3)B为Si元素,其最高价氧化物的分子式为SiO2,故答案为:SiO2.
点评:本题考查位置结构性质关系应用,难度不大,推断元素是解题关键,侧重于化学用语的考查.

练习册系列答案
相关题目
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此下列说法正确的是( )


| A、该硫酸的物质的量浓度为9.2mol/L |
| B、1molZn与足量的该硫酸反应产生2g氢气 |
| C、配制200ml4.6mol/L的稀硫酸需取该硫酸50mL |
| D、该硫酸与等体积的水混合所得溶液的质量分数小于49% |
已知室温下,向浓度均为0.1mol?L-1的HCl、NH4Cl、AlCl3混合溶液中,逐滴加入NaOH溶液.下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是( )
A、 |
B、 |
C、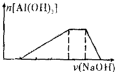 |
D、 |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、2.4 g Mg与足量的盐酸反应失去的电子数为0.2NA |
| B、1 mol?L-1的氨水中含有NH3?H2O的分子数为NA |
| C、11.2L NH3所含有的分子数为0.5 NA |
| D、标准状况下NA 个SO3分子所占有的体积约为22.4L |
减少酸雨产生的途径可采取下列中的哪些措施:①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等⑤开发新能源( )
| A、①②③ | B、②③④⑤ |
| C、①③⑤ | D、①③④⑤ |
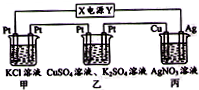
 如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL.
如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL.