题目内容
(10分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:

(1)画出⑧原子结构示意图__________ __;
(2)④、⑤、⑥的简单离子半径由大到小的顺序是________。(用离子符号表示)
(3)①-⑧的元素中,某元素气态氢化物与其最高价氧化物对应的水化物反应所得生成物溶于水,溶液呈酸性,原因是____ _ _(用离子方程式表示),该氢化物分子空间结构为______ _ ;
(4)写出由元素⑥组成的单质与元素⑤最高价氧化物对应的水化物的水溶液反应的离子方程式_ 。
(1) (2)O2->Na++>Al3+ (3)NH4++H2O
(2)O2->Na++>Al3+ (3)NH4++H2O NH3·H2O+H+;三角锥形
NH3·H2O+H+;三角锥形
(4)2Al+2OH-+2H2O=2AlO2-+3H2↑
【解析】
试题分析:根据元素在周期表中的位置可知:①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为Cl,则
(1)氯原子的原子序数是17,其原子结构示意图为 ;
;
(2)O、Na、Al三种元素的简单离子具有相同的核外电子排布,其离子半径随原子序数的增大而减小,因此离子半径大小顺序是O2->Na++>Al3+;
(3)某元素气态氢化物与其最高价氧化物对应的水化物反应所得生成物溶于水,溶液呈酸性,因此该盐是硝酸铵。铵根水解溶液显酸性,离子方程式为NH4++H2O NH3·H2O+H+,氨气的分子空间结构为三角锥形;
NH3·H2O+H+,氨气的分子空间结构为三角锥形;
(4)铝与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。
考点:考查元素周期表与元素周期律的应用

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是
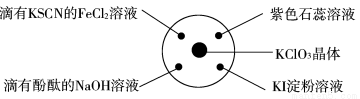
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |


