题目内容
下列实验方案与现象能说明溶液中一定大量存在相应离子的是( )
A、NH4+:试液
| |||||
B、I-:试液
| |||||
C、HCO3-:试液
| |||||
D、Fe2+:试液
|
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:A、氨气和氯化氢反应冒白烟;
B、在酸性环境下,碘离子能被过氧化氢氧化为碘单质;
C、和酸反应能产生使石灰水变浑浊的离子有碳酸根离子、碳酸氢根离子等离子;
D、铁离子遇到硫氰酸根离子显示红色,和氯水之间不会发生反应.
B、在酸性环境下,碘离子能被过氧化氢氧化为碘单质;
C、和酸反应能产生使石灰水变浑浊的离子有碳酸根离子、碳酸氢根离子等离子;
D、铁离子遇到硫氰酸根离子显示红色,和氯水之间不会发生反应.
解答:
解:A、氨气和氯化氢反应冒白烟,但是铵根离子没有该性质,故A错误;
B、在酸性环境下,碘离子能被过氧化氢中氧化为碘单质,碘单质遇到淀粉显示蓝色,故B正确;
C、能和硫酸反应能产生使石灰水变浑浊的离子有碳酸根离子、碳酸氢根离子等离子,故C错误;
D、试液中若是含有三价铁离子,加入氯水无现象,再加入硫氰化钾溶液,也会出现红色,故D错误.
故选B.
B、在酸性环境下,碘离子能被过氧化氢中氧化为碘单质,碘单质遇到淀粉显示蓝色,故B正确;
C、能和硫酸反应能产生使石灰水变浑浊的离子有碳酸根离子、碳酸氢根离子等离子,故C错误;
D、试液中若是含有三价铁离子,加入氯水无现象,再加入硫氰化钾溶液,也会出现红色,故D错误.
故选B.
点评:本题考查学生离子的检验知识,注意离子的特征离子反应是检验离子的关键,难度不大.

练习册系列答案
相关题目
下列关于溶液和胶体的叙述中,正确的是( )
| A、胶体带电荷,而溶液呈电中性 |
| B、胶体加入电解质溶液可产生沉淀,而溶液不能 |
| C、胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系 |
| D、胶体和溶液都能产生丁达尔现象 |
卤素单质从F2到I2在常温常压下的聚集状态由气态、液态到固态的原因是( )
| A、原子间的化学键键能逐渐减小 |
| B、范德华力逐渐增大 |
| C、原子半径逐渐增大 |
| D、氧化性逐渐减弱 |
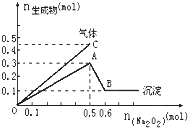 向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )
向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中Mg2+、NH4+、Al3+三种离子的物质的量之比为( )| A、1:1:2 |
| B、2:2:1 |
| C、1:2:2 |
| D、9:2:4 |
下列离子方程式正确的是( )
| A、明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ |
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C、小苏打溶液中加过量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- |
| D、澄清石灰水中通入过量二氧化碳:OH-+CO2=HCO3- |