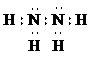题目内容
肼(分子式为N2H4)是火箭发动机的一种燃料.已知8g液态肼与液态双氧水恰好反应,生成氮气与水蒸气,同时放出热量375KJ.下列关于此反应的热化学方程式,正确的是( )
分析:反应方程式为:N2H4+2H2O2=N2+4H2O,根据8g液态肼物质的量=
=0.25mol液态肼放出的热量,计算1mol液态肼放出的热量,标注物质聚集状态和对应焓变进而写出热化学方程式.
| 8g |
| 32g/mol |
解答:解:反应方程式为:N2H4+2H2O2=N2+4H2O,0.25mol液态肼放出375KJ的热量,则1mol液态肼放出的热量为
=1500kJ,
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500kJ/mol,
故选A.
| 375KJ |
| 0.25mol |
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500kJ/mol,
故选A.
点评:本题考查热化学方程式的书写,题目难度不大,注意热化学方程式与化学方程式的区别,生成的水的状态和反应放热判断.

练习册系列答案
相关题目