题目内容
15.氧化还原反应实际上包含氧化和还原两个过程.某氧化还原反应中还原过程的反应式为NO3-+4H++3e-═NO↑+2H2O,下列说法正确的是( )| A. | 选用FeCl2、Cu2O、NaI等物质均能使题中反应发生 | |
| B. | 若用Na2S使题中反应发生则氧化过程的反应式一定为S2-+4H2O-8e-═SO42-+8H+ | |
| C. | 当收集到2.24 L(标准状况下)气体时,参与反应的HNO3为0.1 mol | |
| D. | 若将上述氧化还原反应设计成原电池,则题中反应在负极发生 |
分析 A.要使该反应发生,则需要还原剂;
B.Na2S被氧化为S;
C.硝酸发生氧化还原反应时,作氧化剂,还可能显酸性;
D.原电池中负极失电子.
解答 解:A.要使该反应发生,则需要还原剂,FeCl2、Cu2O、NaI等物质均能作还原剂,所以能使题中反应发生,故A正确;
B.Na2S与硝酸反应生成S沉淀,则发生则氧化过程的反应为S2--2e-═S,故B错误;
C.硝酸发生氧化还原反应时,作氧化剂,还可能显酸性,如Cu2O与硝酸反应生成硝酸铜和NO,所以硝酸不能全部转化为气体,故C错误;
D.原电池中负极失电子,NO3-+4H++3e-═NO↑+2H2O应该为正极的电极反应,故D错误.
故选A.
点评 本题考查了氧化还原反应、原电池原理,明确元素化合价及物质的性质是解本题关键,根据元素化合价来确定物质的性质,题目难度不大.

练习册系列答案
相关题目
20.下列物质中,不能使酚酞溶液变红的是( )
| A. | NH3 | B. | Na2SiO3 | C. | NaHCO3 | D. | Al(OH)3 |
6.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| C. | 2L0.5mol/L亚硫酸溶液中含有的氢离子数为2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
3.将两A、B分别用导线相连接,并同时插入电解质溶液中,发现A极的质量增加,则下列说法正确的是( )
| A. | 金属活动性:A>B | |
| B. | A极是正极,电解质溶液可以是盐酸 | |
| C. | B极是负极 | |
| D. | 要判断A极与B极是正极还是负极,还需考虑电解质溶液 |
20.下列有关溶液中粒子浓度的关系式中,正确的是( )


| A. | pH相同的①CH3COONa;②NaHCO3;③NaAlO2三份溶液中的c(Na+):③>②>① | |
| B. | 25℃时①10-3mol/L的盐酸;②pH=3的NH4Cl溶液;③pH=11的氨水中,水的电离程度为:②>③>① | |
| C. | 图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) | |
| D. | 图中pH=7时c(Na+)>c(CH3COO-)>c(OH-)=c(H+) |
7.实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KMnO4与浓盐酸在常温下反应制备Cl2,下列有关说法中不正确的是( )
| A. | 由题目信息知:KMnO4的氧化性比MnO2的强 | |
| B. | 制备氯气的整个实验过程中,只需要使用氧化剂与还原剂 | |
| C. | 用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体 | |
| D. | 用足量MnO2与含有4 molHCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol |
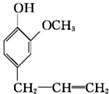 )可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下:
)可用于配制康乃馨型香精以及制异丁香酚和香兰素等,合成丁子香酚的一种路线如下: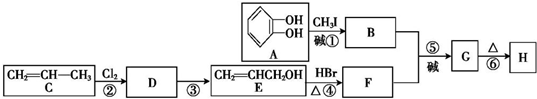
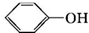 +RX$\stackrel{碱}{→}$
+RX$\stackrel{碱}{→}$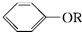 +HX(X代表卤素原子);
+HX(X代表卤素原子);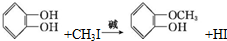 .
. .
.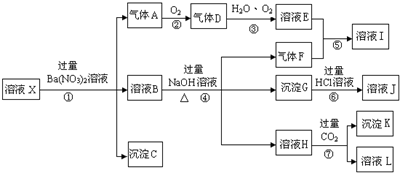
 ,沉淀K的化学式为:Al(OH)3,沉淀G的化学式为:Fe(OH)3,实验中,可以观察到反应②的现象是:气体由无色变红棕色.
,沉淀K的化学式为:Al(OH)3,沉淀G的化学式为:Fe(OH)3,实验中,可以观察到反应②的现象是:气体由无色变红棕色.