题目内容
在100mL0.1mol/L 的醋酸溶液中,欲使醋酸的电离程度增大,H+ 浓度减小,可采用方法是( )
| A、加热 |
| B、加入0.1mol/L 的醋酸溶液100mL |
| C、加入少量的0.5mol/L的硫酸 |
| D、加入少量1mol/L 的NaOH溶液 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:醋酸是弱电解质,弱电解质的电离是吸热反应,升高温度促进其电离,向醋酸中加入和氢离子反应或醋酸根离子反应的物质或者是加水稀释都能促进醋酸电离,但氢离子浓度减小,说明改变的条件能和氢离子反应.
解答:
解:A.醋酸是弱电解质,醋酸的电离是吸热反应,升高温度促进醋酸电离,氢离子浓度增大,所以不符合条件,故A错误;
B.向溶液中加入相同浓度的醋酸溶液,氢离子浓度不变,所以不符合条件,故B错误;
C.向溶液中加入少量硫酸,氢离子浓度增大,抑制醋酸电离,所以不符合条件,故C错误;
D.向溶液中加入少量氢氧化钠溶液,氢氧根离子和氢离子反应,所以促进醋酸电离,且氢离子浓度降低,故D正确;
故选D.
B.向溶液中加入相同浓度的醋酸溶液,氢离子浓度不变,所以不符合条件,故B错误;
C.向溶液中加入少量硫酸,氢离子浓度增大,抑制醋酸电离,所以不符合条件,故C错误;
D.向溶液中加入少量氢氧化钠溶液,氢氧根离子和氢离子反应,所以促进醋酸电离,且氢离子浓度降低,故D正确;
故选D.
点评:本题考查了弱电解质的电离,既要考虑促进醋酸电离又要考虑氢离子浓度降低,根据外界条件对其影响分析解答即可,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的主要成分不是SiO2的是( )
| A、水晶 | B、石英 | C、沙子 | D、干冰 |
25℃某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,在常温下混合后pH=7,则酸溶液体积V酸和碱溶液体积V碱的正确关系为( )
| A、V碱=102V酸 |
| B、V酸=102 V碱 |
| C、V酸=2V碱 |
| D、V碱=2V酸 |
常温下,下列各组数据中比值为2:1的是( )
| A、Na2O2晶体中阴阳离子个数比2:1 |
| B、0.2mol?L-1的CH3COOH溶液与0.1mol?L-1CH3COOH溶液中c(H+)之比 |
| C、pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH4+)与c(SO42-)之比 |
| D、pH=11的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比 |
工业上制造金刚砂(SiC)的化学反应如下:SiO2+3C═SiC+2CO↑,在这个反应中,氧化剂和还原剂的物质的量之比是( )
| A、1:2 | B、2:1 |
| C、1:1 | D、3:1 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4↓+2H2O,根据此反应判断下列叙述中正确是( )
| A、PbO2是电池的负极 |
| B、负极的电极反应式为:Pb+SO42--2e -=PbSO4↓ |
| C、PbO2得电子,被氧化 |
| D、电池放电时,溶液酸性增强 |
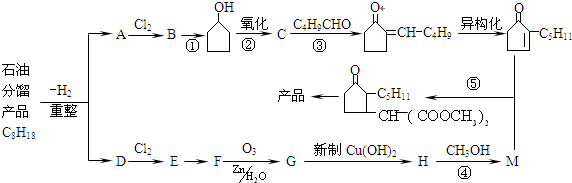
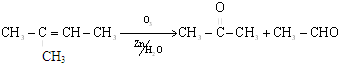 从石油分馏产品C8H18制取二氢茉莉酮酸甲酯(香料)的流程如图:(备注:E是D的一元取代物)
从石油分馏产品C8H18制取二氢茉莉酮酸甲酯(香料)的流程如图:(备注:E是D的一元取代物)