题目内容
19. 硫-碘循环分解水制氢主要涉及下列反应:
硫-碘循环分解水制氢主要涉及下列反应:I SO2+2H2O+I2═H2SO4+2HI
II 2HI?H2+I2
III 2H2SO4═2SO2+O2+2H2O(1)分析上述反应,下列判断正确的是c.
a.反应III易在常温下进行 b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2Od.循环过程中产生1molO2的同时产生1molH2
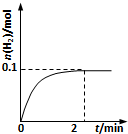
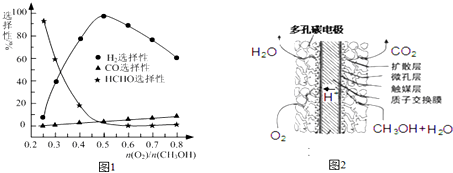
(2)一定温度下,向1L密闭容器中加入1molHI(g),发生反应II,H2物质的量随时间的变化如图所示.0~2min内的平均反应速率v(HI)=0.1mol•L-1•min-1.该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=64.相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则b是原来的2倍.
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡向右移动(填“向左”“向右”或“不”);若加入少量下列试剂中的b,产生H2的速率将增大.
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池.
已知 2H2(g)+O2(g)=2H2O(l)△H=-572kJ•mol-1
某氢氧燃料电池释放228.8kJ电能时,生成1mol液态水,该电池的能量转化率为80%.
分析 (1)a.硫酸常温下,不易分解.
b.反应中二氧化硫表现还原性,氧化性比HI强.
c.1molSO2消耗2molH2O生成1molH2SO4,1molH2SO4分解生成1molSO2与1molH2O.
d.由Ⅲ可知产生lmolO2的同时产生2molSO2,由I可知2molSO2生成4molHI,由Ⅱ可知4molHI分解生成2mol H2.
(2)由图可知,2min内H2物质的量的变化量,然后计算化学反应速率,再利用化学反应速率之比等于化学计量数之比来解答;根据反应方程式写平衡表达式,结合平衡浓度计算平衡常数,化学方程式改变方向,平衡常数互为倒数;利用浓度对化学平衡的影响来分析HI的平衡浓度、达到平衡的时间、平衡时H2的体积分数,但温度不变,平衡常数不变;
(3)实验室用Zn和稀硫酸制取H2,随反应进行氢离子浓度减小,反应时溶液中水的电离平衡正向进行;依据影响化学反应速率因素分析判断增大反应速率的试剂,注意原电池反应的分析判断;
(4)先根据热化学方程式式求出生成1mol液态水,理论上放出的能量,然后根据电池的能量转化率=$\frac{实际生成量}{理论生成量}$×100%;
解答 解:(1)a.硫酸常温下温度,不易分解,故a错误;
b.反应中二氧化硫表现还原性,还原性比HI强,碘单质氧化性大于二氧化硫,故b错误;
c.1molSO2消耗2molH2O生成1molH2SO4,1molH2SO4分解生成1molSO2与1molH2O,循环中水的量减少,故应补充水,故c正确;
d.由Ⅲ可知产生lmolO2的同时产生2molSO2,由I可知2molSO2生成4molHI,由Ⅱ可知4molHI分解生成2mol H2,即循环过程中产生l mol O2的同时产生2mol H2,故d错误;
故选:c;
(2)由图可知2min内氢气的物质的量增加了0.1mol,则氢气的浓度为$\frac{0.1mol}{1L}$=0.1mol/L,用氢气表示的化学反应速率为$\frac{0.1mol/L}{2min}$=0.05mol/(L.min),
由反应中的化学计量数可知v(HI)=0.05mol/(L.min)×2=0.1mol/(L.min);根据方程式计算平衡浓度,c(H2)=0.1mol/L,c(I2)=0.1mol/L,c(HI)=0.8mol/L,写出平衡常数表达式计算:K=$\frac{c(H{\;}_{2})c(I{\;}_{2})}{c{\;}^{2}(HI)}$=$\frac{0.1×0.1}{0.8{\;}^{2}}$=$\frac{1}{64}$,则该温度下,H2(g)+I2(g)?2HI(g)的平衡常数K=64;
对该反应,当温度不变开始加入HI(g)的物质的量是原来的2倍,则温度不变,K不变,故a错;物质的量为原来的2倍,该反应是反应前后气体体积相等的反应,则反应体系中各物质的浓度都是原来的2倍,故b正确;物质的量增大,则化学反应速率先增大的快,后随浓度的减小,速率增大的程度变小,故c错;由反应方程式及原来的量与后来的量成正比,则这两种情况下建立的平衡为等效平衡,即平衡时H2的体积分数相同,故d错;
故答案为:0.1mol•L-1•min-1;64;b;
(3)实验室用Zn和稀硫酸制取H2,反应过程中氢离子浓度减小,反应时溶液中水的电离平衡正向进行,若加入少量下列试剂中生成氢气反应速率增大的是;
a.加入NaNO3 溶液相当于稀释溶液浓度减小,反应速率减小,故a不符合;
b.加入CuSO4 溶液,和锌反应生成铜,铜和锌在稀硫酸溶液中形成原电池反应,生成氢气速率增大,故b符合;
c.加入Na2SO4溶液相当于稀释溶液浓度减小,反应速率减小,故c不符合;
d.加入NaHSO3 溶液会消耗硫酸,生成氢气的反应速率减小,故d不符合;
故答案为:向右;b;
(4)生成1mol液态水,理论上放出的能量为$\frac{572KJ}{2}$=286KJ,电池的能量转化率=$\frac{实际生成量}{理论生成量}$×100%=$\frac{228.8KJ}{286KJ}$×100%=80%,故答案为:80%.
点评 本题主要考查了反应方程式的分析及计算,反应平衡图象,平衡常数、反应速率概念计算应用,难度中等.对于图象,要看清图象的含义、拐点、平衡点,结合平衡移动规律进行判断.

 阅读快车系列答案
阅读快车系列答案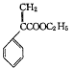 )是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,下列说法正确的是( )
)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,下列说法正确的是( )| A. | 不能使酸性KMnO4溶液褪色 | |
| B. | 1mol颠茄酸酯最多与4molBr2发生加成反应 | |
| C. | 能与NaHCO3溶液反应 | |
| D. | 能与NaOH溶液反应 |
| A. | 当a≤100时,发生的离子反应为:OH-+H+=H2O | |
| B. | 当a≥300时,发生的离子反应为:OH-+3H++CO32-=2H2O+CO2↑ | |
| C. | 当100<a<200时,反应后的溶液中CO32-与HCO3-的物质的量之比为(a×10-4-0.01):(0.02-a×10-4) | |
| D. | 当a=200时,发生的离子反应为:OH-+2H++CO32-=H2O+HCO3- |
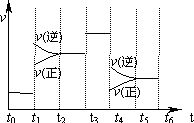
| A. | t2~t3和t3~t4时间段氨气的体积分数相等 | |
| B. | 氨气的体积分数最高的一段时间为t5~t6 | |
| C. | t4时刻改变的条件是降低温度 | |
| D. | t4~t5时间段平衡向正反应方向移动 |
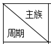 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
(2)A、C、D 三种元素的最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式).
(3)A、B、C 三种元素的阳离子按离子半径由大到小的顺序排列为K+>Na+>Mg2+.(用元素的离子符号表示).
(4)X 元素是 A~R 十种元素中的一种,X 的氢氧化物既能与氢氧化钠溶液反应,又能与盐酸反应.则 X 的最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 工业上通常用电解Na、Mg、Al对应的氯化物制取三种金属单质 | |
| C. | 燃料电池中燃料都是在负极发生氧化反应 | |
| D. | Fe3O4俗称铁红,常作红色油漆和涂料 |
| A. |  长颈漏斗 | B. |  表面皿 | C. |  三脚架 | D. |  瓷钳锅 |
 W、X、Y、Z、M、Q均为稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的电子总数的4倍,Z与M最外层电子数相同,X与M在周期表中的位置如图:
W、X、Y、Z、M、Q均为稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的电子总数的4倍,Z与M最外层电子数相同,X与M在周期表中的位置如图: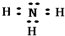 .
.