题目内容
计算:
(1)在0.5molH2O中,所含有分子数 ,原子数 ,电子数 .
(2)标准状况下:5.6LO2的物质的量是 ,质量是 .
(3)将58.5g的NaCl配制成2L溶液,该溶液的物质的量的浓度为 .
(1)在0.5molH2O中,所含有分子数
(2)标准状况下:5.6LO2的物质的量是
(3)将58.5g的NaCl配制成2L溶液,该溶液的物质的量的浓度为
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
结合分子的构成特点计算;
(2)根据n=
=
计算;
(3)计算出溶质的物质的量,结合c=
计算.
| N |
| NA |
(2)根据n=
| V |
| Vm |
| m |
| M |
(3)计算出溶质的物质的量,结合c=
| n |
| V |
解答:
解:(1)在0.5molH2O中,所含有分子数为0.5 NA,因每个分子含有3个原子,则含有的原子数为1.5 NA,每个分子含有10个电子,则含有的电子数为5 NA,
故答案为:0.5 NA;1.5 NA;5 NA;
(2)n(O2)=
=0.25mol,m(O2)=0.25mol×32g/mol=8g,故答案为:0.25mol;8g;
(3)n(NaCl)=
=1mol,c(NaCl)=
=0.5mol/L,故答案为:0.5mol/L.
故答案为:0.5 NA;1.5 NA;5 NA;
(2)n(O2)=
| 5.6L |
| 22.4L/mol |
(3)n(NaCl)=
| 58.5g |
| 58.5g/ml |
| 1mol |
| 2L |
点评:本题考查较为综合,多角度考查物质的量的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
相关题目
下列说法错误的是( )
| A、丁达尔效应可以区分溶液和胶体 |
| B、一种分散系里只能有一种分散质 |
| C、以水为分散剂的分散系,按稳定性由弱至强的顺序是:浊液?胶体?溶液 |
| D、分散系中分散质粒子直径由大到小的顺序是:浊液?胶体?溶液 |

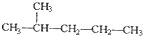 和
和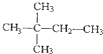 ②
② 和
和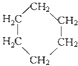
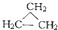 ④C2H6和
④C2H6和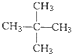 ⑤
⑤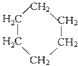 和
和