题目内容
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA |
| B、1L 1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
| C、质量a g的C2H4和C3H6的混合物中共用电子对数目为3a NA/14 |
| D、常温下,pH=13的NaOH溶液中含有OH一的数目为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氮气和一氧化碳的摩尔质量都是28g/mol,14g混合气体的物质的量为0.5mol,含有1mol原子;
B.次氯酸钠溶液中,次氯酸根离子部分水解,溶液中次氯酸根离子数目减少;
C.C2H4和C3H6的最简式为CH2,根据最简式计算出混合物中含有的C、H原子的物质的量,再根据有机物成键1情况判断含有的共用电子对数目;
D.缺少氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目.
B.次氯酸钠溶液中,次氯酸根离子部分水解,溶液中次氯酸根离子数目减少;
C.C2H4和C3H6的最简式为CH2,根据最简式计算出混合物中含有的C、H原子的物质的量,再根据有机物成键1情况判断含有的共用电子对数目;
D.缺少氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目.
解答:
解:A.14g氮气和一氧化碳的物质的量为0.5mol,0.5mol二者的混合气体中含有1mol原子,含有的原子数目为NA,故A错误;
B.1L 1mol?L-1的NaClO溶液中含有溶质次氯酸钠1mol,由于次氯酸根离子部分水解,溶液中次氯酸根离子的物质的量小于1mol,含有的ClO-的数目小于NA,故B错误;
C.C2H4和C3H6中,每个C原子平均形成了1对碳碳共用电子对、每个H原子平均形成了1对碳氢共用电子对,a g的C2H4和C3H6的混合物中含有
mol最简式CH2,含有
molC、
molH原子,含有的共用电子对为:
mol+
mol=
mol,含有的共用电子对数为
NA,故C正确;
D.没有告诉pH=13的NaOH溶液的体积,无法计算溶液中氢氧根离子的物质的量,故D错误;
故选C.
B.1L 1mol?L-1的NaClO溶液中含有溶质次氯酸钠1mol,由于次氯酸根离子部分水解,溶液中次氯酸根离子的物质的量小于1mol,含有的ClO-的数目小于NA,故B错误;
C.C2H4和C3H6中,每个C原子平均形成了1对碳碳共用电子对、每个H原子平均形成了1对碳氢共用电子对,a g的C2H4和C3H6的混合物中含有
| a |
| 14 |
| a |
| 14 |
| a |
| 7 |
| a |
| 14 |
| a |
| 7 |
| 3a |
| 14 |
| 3a |
| 14 |
D.没有告诉pH=13的NaOH溶液的体积,无法计算溶液中氢氧根离子的物质的量,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确盐的水解原理,选项D为易错点,注意题中缺少溶液体积.

练习册系列答案
相关题目
下列热化学方程式正确的是( )
| A、甲烷的标准燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 | ||
| B、稀HNO3溶液与NaOH溶液发生反应生成1 mol H2O时放出57.3 kJ的热量.其热化学方程式为:HNO3(l)+NaOH(l)=NaNO3(l)+H2O(l)△H=-57.3 kJ?mol-1 | ||
| C、若:2H2S(g)+O2(g)═2S(s)+2H2O(l)△H=-Q kJ?mol-1.则:2H2S(g)+O2(g)═2S(s)+2H2O(g)△H<-Q kJ?mol-1 | ||
D、若:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1;Na2O2(s)+CO2(g)═Na2CO3(s)+
|
NaCl溶液中含有少许Na2SO4,加入下列哪种试剂可除去其中的Na2SO4( )
| A、BaCl2 |
| B、KCl |
| C、H2SO4 |
| D、HCl |
下列不属于官能团的是( )
| A、-Br |
| B、OH- |
| C、-CHO |
D、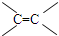 |
下列各组气体中,在常温常压下,能在同一容器中共存的是( )
| A、SO2、H2、O2 |
| B、SO2、H2S、H2 |
| C、NO、NO2、O2 |
| D、NH3、N2、HCl |
下列实验方法能达到目的是( )
| A、用氨水清洗试管内壁附着的银镜 |
| B、用饱和Na2CO3溶液除去乙醇中少量的乙酸和水 |
| C、制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| D、可用K3[Fe(CN)6]溶液鉴定FeCl3溶液中是否存在Fe2+ |
下列病患是由于缺乏维生素引起的是( )
| A、坏血病 | B、佝偻病 |
| C、贫血 | D、呆小症 |
钓鱼岛是我国固有领土,钓鱼岛海域附近储藏着大量石油和其他海洋资源.下列关于石油的说法正确的是( )
| A、石油属于可再生矿物能源 |
| B、石油分馏的各馏分均是纯净物 |
| C、石油的裂化是物理变化 |
| D、石油主要含有碳、氢两种元素 |