题目内容
在一定条件下的密闭容器中,进行反应:2SO2(g)+O2(g)?2SO3(g).下列有关说法正确的是( )
| A、催化剂的使用可实现SO2的转化率为100% |
| B、达到化学平衡时,各物质的浓度不再改变 |
| C、其他条件不变,升高温度,不能增大反应的速率 |
| D、其他条件不变,降低SO3的浓度,可以增大反应的速率 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A.催化剂不影响平衡移动;
B.可逆反应达到平衡状态时,各物质的浓度不变;
C.其他条件不变,升高温度,正逆反应速率都增大;
D.其他条件不变,降低SO3的浓度,反应速率减小.
B.可逆反应达到平衡状态时,各物质的浓度不变;
C.其他条件不变,升高温度,正逆反应速率都增大;
D.其他条件不变,降低SO3的浓度,反应速率减小.
解答:
解:A.催化剂只改变反应速率,不影响平衡移动,且可逆反应达到平衡状态时存在动态平衡,所以反应物不可能完全转化为生成物,故A错误;
B.达到平衡状态时,正逆反应速率相等,可逆反应存在动态平衡,导致各物质的百分含量不变,则各物质的浓度不再改变,故B正确;
C.其他条件不变,升高温度,活化分子百分数增大,导致正逆反应速率都增大,故C错误;
D.其他条件不变,降低SO3的浓度,反应速率减小,故D错误;
故选B.
B.达到平衡状态时,正逆反应速率相等,可逆反应存在动态平衡,导致各物质的百分含量不变,则各物质的浓度不再改变,故B正确;
C.其他条件不变,升高温度,活化分子百分数增大,导致正逆反应速率都增大,故C错误;
D.其他条件不变,降低SO3的浓度,反应速率减小,故D错误;
故选B.
点评:本题考查了化学平衡的影响因素,明确温度、浓度、压强对化学平衡影响的原理,改变压强是通过改变浓度来影响平衡移动的,知道催化剂不影响平衡移动,只改变速率,注意:无论可逆反应是吸热反应还是放热反应,升高温度时化学反应速率都增大,为易错点.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
下列金属或氧化物可以完全溶解的是( )
| A、1mol Zn与含1mol HCl的稀盐酸共热 |
| B、1mol Cu与含2mol H2SO4的浓硫酸共热 |
| C、1mol Cu与含4mol HNO3的浓硝酸 |
| D、1mol MnO2与含4mol HCl的浓盐酸共热 |
2012年4月22日是第43个“世界地球日”,其主题为.“绿色梦想,低碳行动”.下列做法符合这一主题的是( )
①开发太阳能、风能和氢能等能源;②推广“煤气化”技术以提高煤的利用率;③在含硫的煤中加入适量生石灰;④利用苯、甲苯等有机物代替水作溶剂;⑤利用可降解的“玉米塑料”生产一次性饭盒.
①开发太阳能、风能和氢能等能源;②推广“煤气化”技术以提高煤的利用率;③在含硫的煤中加入适量生石灰;④利用苯、甲苯等有机物代替水作溶剂;⑤利用可降解的“玉米塑料”生产一次性饭盒.
| A、①②③⑤ | B、①②③④ |
| C、②③④⑤ | D、①②④⑤ |
下列物质中属于电解质的是( )
| A、二氧化碳 | B、银 |
| C、硫酸钡 | D、烧碱溶液 |
下列化合物中,既能由单质直接化合制得,又能由复分解反应制得的是( )
| A、CuS |
| B、FeS |
| C、Al2S3 |
| D、FeCl2 |
某高分子化合物的结构简式为 ,该物质可由下列哪组物质为原料直接合成得到( )
,该物质可由下列哪组物质为原料直接合成得到( )
 ,该物质可由下列哪组物质为原料直接合成得到( )
,该物质可由下列哪组物质为原料直接合成得到( )A、 和CH3CH2OH 和CH3CH2OH |
B、 和HOCH2CH2OH 和HOCH2CH2OH |
C、 和CH3CH2OH 和CH3CH2OH |
D、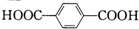 和HOCH2CH2OH 和HOCH2CH2OH |
 Ⅰ.已知:温度过高时,WO2(s)转变为WO2(g):
Ⅰ.已知:温度过高时,WO2(s)转变为WO2(g):