题目内容
用下列实验装置进行相应实验,设计正确且能达到实验目的是( )
A、 用装置制取少量H2: |
B、 用装置分离Na2CO3溶液和CH3COOC2H5的混合物 |
C、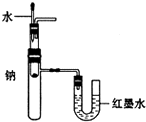 用装置验证Na和水反应的热效应 |
D、 用装置蒸干A1Cl3溶液制备无水AlC13 |
考点:化学实验方案的评价
专题:
分析:A.制取氢气时需要用分液漏斗或将长颈漏斗伸入液面下;
B.蒸馏时,温度计测定馏分温度,互不相溶的液体可以采用分液方法分离;
C.利用产生的压强差判断反应热;
D.氯化铝水解生成氢氧化铝和HCl,升高温度促进HCl挥发,从而促进氯化铝水解.
B.蒸馏时,温度计测定馏分温度,互不相溶的液体可以采用分液方法分离;
C.利用产生的压强差判断反应热;
D.氯化铝水解生成氢氧化铝和HCl,升高温度促进HCl挥发,从而促进氯化铝水解.
解答:
解:A.制取氢气时需要用分液漏斗或将长颈漏斗伸入液面下,如果用该装置制取氢气,生成的氢气易从漏掉中逸出,故A错误;
B.蒸馏时,温度计测定馏分温度,互不相溶的液体可以采用分液方法分离,碳酸钠溶液和乙酸乙酯不互溶,应该采用分液方法分离,故B错误;
C.利用产生的压强差判断反应热,根据U型管中液体判断试管中压强变化,气体具有热胀冷缩性质,所以该装置能判断钠的反应热,故C正确;
D.氯化铝水解生成氢氧化铝和HCl,升高温度促进HCl挥发,从而促进氯化铝水解,低温蒸干溶液最终得到氢氧化铝,故D错误;
故选C.
B.蒸馏时,温度计测定馏分温度,互不相溶的液体可以采用分液方法分离,碳酸钠溶液和乙酸乙酯不互溶,应该采用分液方法分离,故B错误;
C.利用产生的压强差判断反应热,根据U型管中液体判断试管中压强变化,气体具有热胀冷缩性质,所以该装置能判断钠的反应热,故C正确;
D.氯化铝水解生成氢氧化铝和HCl,升高温度促进HCl挥发,从而促进氯化铝水解,低温蒸干溶液最终得到氢氧化铝,故D错误;
故选C.
点评:本题考查化学实验方案评价,为高考高频点,涉及物质的分离和提纯、反应热、盐类水解、物质的制备等知识点,明确实验原理是解本题关键,知道物质的性质及常见物质分离方法,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
常温下,0.1 mol?L-1CH3COONa溶液pH=a,则下列说法正确的是( )
| A、CH3COOH在常温下Ka数值约为l×101-2a |
| B、约有1.0×l0a-14 mol?L-1的水发生电离 |
| C、加热后溶液pH<a |
| D、加少量水后,溶液pH>a |
某有机物的结构简式如图所示,下列有关该有机物的说法中正确的是( )


| A、能和碳酸钠溶液反应的官能团有2种 |
| B、1mol该有机物最多能与2molH2发生加成 |
C、与 互为同分异构体 互为同分异构体 |
| D、既可以发生取代反应又可以发生氧化反应 |
下列各组离子一定能大量共存的是( )
| A、含大量Fe3+的溶液中:NH4+、Mg2+、Cl-、HSO3- |
| B、加入Al有H2生成的溶液中:Na+、K+、Cl-、NO3- |
| C、NaOH溶液中:K+、Na+、AlO2-、CO32- |
| D、NaHCO3溶液中:K+、Al3+、Cl-、SO42-、 |


