题目内容
4.将11.2L标准状况下的甲烷和乙烯的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了5.6g,求原混合气体中甲烷与乙烯的物质的量之比和质量之比.分析 乙烯与溴发生加成反应,溴的四氯化碳溶液增加的质量为乙烯的质量,计算混合气体、乙烯的物质的量,进而计算甲烷的物质的量,再计算甲烷的质量,据此解答.
解答 解:乙烯与溴发生加成反应,溴的四氯化碳溶液增加的质量为5.6g,则:m(C2H4)=5.6g,n(C2H4)=$\frac{5.6g}{28g/mol}$=0.2mol,
而n(CH4)+n(C2H4)=$\frac{11.2L}{22.4l/mol}$=0.5mol,所以n(CH4)=0.5mol-0.2mol=0.3mol,故m(CH4)=0.3mol×16g/mol=4.8g,
故原混合气体中甲烷与乙烯的质量之比=4.8g:5.6g=6:7,
答:原混合气体中甲烷与乙烯的物质的量之比为3:2,原混合气体中甲烷与乙烯的质量之比为6:7.
点评 本题考查混合物计算,比较基础,关键是明确乙烯与溴发生加成反应确定乙烯的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
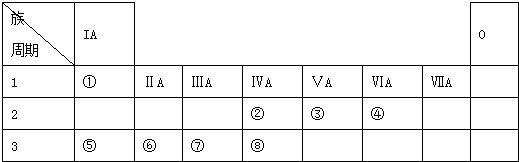
12.现有下列短周期元素部分性质的数据:
请回答下列问题:
(1)②和⑧两元素所对应的氢化物,最稳定的是HF(填化学式);
(2)③和⑥两元素的最高价氧化物对应水化物的反应是放热(填“放热”或“吸热”)反应;
(3)①⑤⑦三种元素的最高价氧化物对应水化物,酸性由强到弱的顺序是H2CO3>H2SiO3>Al(OH)3(填化学式).
| 编号 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径/10-10m | 0.77 | 0.99 | 1.86 | 0.75 | 1.17 | 1.02 | 1.43 | 0.71 | 1.52 | 0.89 |
| 最高正化合价 | +4 | +7 | +1 | +5 | +4 | +6 | +3 | +1 | +2 | |
| 最低负化合价 | -4 | -1 | -3 | -4 | -2 | -1 |
(1)②和⑧两元素所对应的氢化物,最稳定的是HF(填化学式);
(2)③和⑥两元素的最高价氧化物对应水化物的反应是放热(填“放热”或“吸热”)反应;
(3)①⑤⑦三种元素的最高价氧化物对应水化物,酸性由强到弱的顺序是H2CO3>H2SiO3>Al(OH)3(填化学式).
19.下列说法正确的是( )
| A. | H2、D2和T2互称为同素异形体 | B. | 35Cl和37Cl 互称为同位素 | ||
| C. |  和 和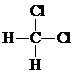 互称为同分异构体 互称为同分异构体 | D. | C2H4与C4H8一定能互称为同系物 |
9.下列物质中只含有离子键的是( )
| A. | MgCl2 | B. | NH4Cl | C. | CO2 | D. | NaOH |
16.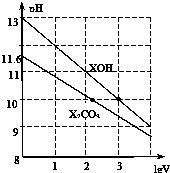 体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
 体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )| A. | XOH是强碱 | |
| B. | pH=10的两种溶液中的c(X+):XOH大于X2CO3 | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1×10-10•2 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$减小 |
14.下列离子方程式书写正确的是( )
| A. | 铁跟稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 钠跟水反应 Na+H2O═Na++OH-+H2↑ | |
| C. | 大理石跟稀盐酸反应 CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 氯气通入水中 Cl2+H2O═2H++Cl-+ClO- |
 或
或 .
.
 .
.