题目内容
1.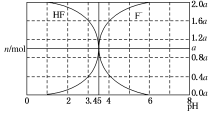 25℃时,用 2a mol•L-1 NaOH 溶液滴定 1.0L 2a mol•L-1氢氟酸溶液,得到混合液中 HF、F-的物质的量与溶液 pH 的变化如图所示.下列说法正确的是( )
25℃时,用 2a mol•L-1 NaOH 溶液滴定 1.0L 2a mol•L-1氢氟酸溶液,得到混合液中 HF、F-的物质的量与溶液 pH 的变化如图所示.下列说法正确的是( )| A. | pH=3 时,溶液中:c(Na+)>c(F-) | |
| B. | c(F-)>c(HF)时,溶液一定呈碱性 | |
| C. | pH=4 时,溶液中:c(HF)+c(Na+)+c(H+)-c(OH-)<2a mol?L-1 | |
| D. | pH=3.45 时,NaOH 溶液恰好与 HF 完全反应 |
分析 A.pH=3时,c(H+)>c(OH-),结合溶液中电荷守恒判断;
B.当pH>3.45时,c(F-)>c(HF),结合图象分析;
C.可根据pH=4时,混合溶液体积大于1.0L,c(F-)<1.6amol/L,c(HF)<0.4amol/L,结合溶液中电荷守恒判断;
D.HF为弱酸,恰好反应时溶液应成碱性.
解答 解:A.pH=3时,c(H+)>c(OH-),溶液中存在:c(Na+)+c(H+)=c(OH-)+c(F-),则c(F-)>c(Na+),故A错误;
B.当pH>3.45时,c(F-)>c(HF),溶液可能呈酸性、中性或碱性,故B错误;
C.当pH=4时,混合溶液体积大于1.0L,c(F-)<1.6amol/L,c(HF)<0.4amol/L,溶液中存在:c(Na+)+c(H+)=c(OH-)+c(F-),c(F-)=c(Na+)+c(H+)-c(OH-)<1.6amol/L,则c(HF)+c(Na+)+c(H+)-c(OH-)<2amol•L-1,故C正确;
D.HF为弱酸,恰好反应时溶液应成碱性,当pH=3.45时,HF酸过量,故D错误.
故选C.
点评 本题考查酸碱混合的计算和判断,题目难度中等,注意把握图象的曲线变化特点,为解答该题的关键,注意HF为弱电解质的特点.

练习册系列答案
相关题目
11. 最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生产锂离子电池.下列说法正确的是( )
最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生产锂离子电池.下列说法正确的是( )
 最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生产锂离子电池.下列说法正确的是( )
最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生产锂离子电池.下列说法正确的是( )| A. | 图中能量化方式只有一种 | |
| B. | 阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑ | |
| C. | 若反应中转移1mole-,则理论上消耗CO32-0.5mol | |
| D. | 当生成12g碳材料时,可收集到22.4L O2 |
12.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如图(废料中含Al、Li、Co2O3和Fe2O3等物质)
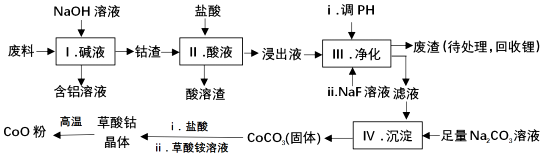
已知:①物质溶解性:LiF难溶于水;LiCO3微溶于水;CoCO3难溶于水
②部分金属离子形成氢氧化物沉淀的pH见表一.
表一:
请回答:
(1)I中得到含铝溶液的反应离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)I中得到钴渣的实验操作是过滤(填操作名称).
(3)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(4)步骤Ⅲ中调节溶液的pH时,pH的范围是3.2≤PH<7.15
(5)废渣中的主要成分有Fe(OH)3,LiF.步骤Ⅲ中加入NaF溶液,对步骤Ⅳ所起的作用是降低溶液中Li+的浓度,避免步骤Ⅳ形成Li2CO3的沉淀.
(6)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表二.已知[M(CoC2O4•2H2O)]=183g/mol
表二:
①加热到210℃时,固体物质的化学式为:CoC2O4
②经测定,加热到210~310℃过程中生成物只有CO2和钴的氧化物,此过程发生反应的化学方程式为:3CoC2O4+2O2$\frac{\underline{\;210~310℃\;}}{\;}$Co3O4+6CO2.

已知:①物质溶解性:LiF难溶于水;LiCO3微溶于水;CoCO3难溶于水
②部分金属离子形成氢氧化物沉淀的pH见表一.
表一:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)I中得到含铝溶液的反应离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)I中得到钴渣的实验操作是过滤(填操作名称).
(3)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(4)步骤Ⅲ中调节溶液的pH时,pH的范围是3.2≤PH<7.15
(5)废渣中的主要成分有Fe(OH)3,LiF.步骤Ⅲ中加入NaF溶液,对步骤Ⅳ所起的作用是降低溶液中Li+的浓度,避免步骤Ⅳ形成Li2CO3的沉淀.
(6)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表二.已知[M(CoC2O4•2H2O)]=183g/mol
表二:
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
②经测定,加热到210~310℃过程中生成物只有CO2和钴的氧化物,此过程发生反应的化学方程式为:3CoC2O4+2O2$\frac{\underline{\;210~310℃\;}}{\;}$Co3O4+6CO2.
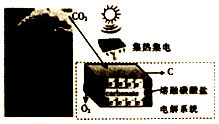
9. 我国科学家最近发明“可充电Na-CO2电池”,示意图如图.该电池的工作原理为:4Na+3CO2$?_{放电}^{充电}$2Na2CO3+C.下列说法错误的是( )
我国科学家最近发明“可充电Na-CO2电池”,示意图如图.该电池的工作原理为:4Na+3CO2$?_{放电}^{充电}$2Na2CO3+C.下列说法错误的是( )
 我国科学家最近发明“可充电Na-CO2电池”,示意图如图.该电池的工作原理为:4Na+3CO2$?_{放电}^{充电}$2Na2CO3+C.下列说法错误的是( )
我国科学家最近发明“可充电Na-CO2电池”,示意图如图.该电池的工作原理为:4Na+3CO2$?_{放电}^{充电}$2Na2CO3+C.下列说法错误的是( )| A. | 放电时,Na+由钠箔端向多壁碳纳米管端移动 | |
| B. | 放电时,正极的电极反应为:3CO2+4Na++4e-═2Na2CO3+C | |
| C. | 该电池不宜在高温下使用 | |
| D. | 充电时,钠箔与外接电源的正极相连 |
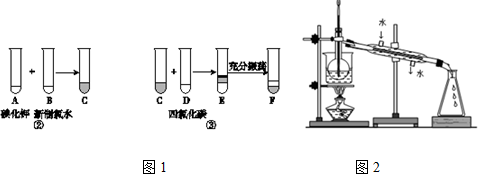
16.下列关于实验现象的描述正确的是( )
| A. | 往碘化钠溶液中加入新制氯水可看到有紫黑色固体生成 | |
| B. | 向盛有1mLmol/LMgCl2溶液的试管中滴加1-2滴2mol/LNaOH溶液,有白色沉淀产生,再滴加2滴0.1mol/LFeCl3溶液,白色沉淀转变为红褐色 | |
| C. | 重铬酸钾酸性溶液中加入乙醇,溶液由墨绿色变为橙黄色 | |
| D. | 用石墨作电极电解CuCl2溶液可观察到阳极石墨棒上覆盖一层红色的铜,阴极石墨棒上生成能使湿润碘化钾淀粉试纸变蓝的气体 |
6.“千锤万凿出深山,烈火焚烧若等闲.粉身碎骨浑不怕,只要留清白在人间“明代诗人于谦的《石灰吟》中对“CaCO3→CaO”的转化进行拟人化的描述,下列说法正确的是( )
| A. | 上述转化属于分解反应 | B. | 上述反应过程放出大量热 | ||
| C. | 生成的CaO可作氯气的干燥剂 | D. | CaCO3水泥的主要成分之一. |
13.Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | Na2S有强还原性 | 用于除去废水中的Cu2+和Hg2+ |
| B | 浓H2SO4有强氧化性 | 浓H2SO4可用于干燥SO2 |
| C | NaHCO3溶于水完全电离 | NaHCO3是强电解质 |
| D | Cl2具有酸性 | Cl2可与石灰乳或烧碱反应制备含氯消毒剂 |
| A. | A | B. | B | C. | C | D. | D |