题目内容
18. 气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.如表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )
气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.如表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )| 待测气体 | 部分电极反应产物 |
| CO | CO2 |
| H2S | H2SO4 |
| Cl2 | HCl |
| N2O4 | NO |
| A. | 上述气体检测时,敏感电极均作电池负极 | |
| B. | 检测Cl2气体时,敏感电极的电极反应式为Cl2+2e-═2Cl- | |
| C. | 检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2+4e-═2O2- | |
| D. | 检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同 |
分析 A.失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极;
B.检测氯气时,氯气得电子生成氯离子;
C.检测硫化氢时,硫化氢生成硫酸,硫元素发生氧化反应,则其所在电极为负极;
D.产生的电流大小与失电子多少有关.
解答 解:A.失电子发生氧化反应的电极是负极、得电子发生还原反应的电极是正极,根据待测气体和反应产物可知,部分气体中元素化合价上升,部分气体中元素的化合价下降,所以敏感电极不一定都做电池正极,故A错误;
B.检测氯气时,氯气得电子生成氯离子,电极反应式为Cl2+2e-═2Cl-,故B正确;
C.检测硫化氢时,硫化氢生成硫酸,硫元素化合价由-2价变为+6价而发生氧化反应,则其所在电极为负极,正极上氧气得电子和氢离子反应生成水,电极电极反应式为O2+4H++4e-═2H2O,故C错误;
D.产生的电流大小与失电子多少有关,检测H2S和CO体积分数相同的两份空气样本时,硫化氢失去电子数大于CO,所以产生电流大小不同,故D错误;
故选B.
点评 本题考查了原电池原理,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意根据元素化合价变化确定正负极,正确判断正负极是解本题关键,难点是电极反应式的书写,注意产生电流与相同物质的量的物质得失电子多少有关,为易错点.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
8.在一个1L的密闭容器中,加入2molA和1molB,发生下述反应:2A(g)+B(g)?3C(g)+D(s),达到平衡时,C的浓度为1.2mol/L,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2mol/L的是( )
| A. | 1mol A+0.5mol B+1.5mol C+0.1mol D | |
| B. | 3mol C+0.5mol D | |
| C. | 2mol A+1mol B+1molD | |
| D. | 0.5mol A+0.25mol B+2.25mol C |
6.25℃时,某溶液中可能含以下几种离子:Na+、H+、Fe3+、HCO3-、OH-、I-.已知溶液中由水电离出的c(H+)=10-13mol•L-1,向该溶液中通入一定量的Cl2后,溶液由无色变为黄色,下列有关该溶液的说法中正确的是( )
| A. | 该溶液的pH一定等于1 | |
| B. | 阴离子肯定有I-,不能确定有无HCO3- | |
| C. | 阳离子肯定没有Fe3+,可能有Na+ | |
| D. | 该溶液含有的溶质成分可能为HI或HI和NaI或NaI和NaOH或NaI |
13.若mg Na在足量氯气中燃烧,生成固体的质量为(m+3.55g),则mg Na与氧气反应,生成固体的质量为 ( ) ①(m+0.8g) ②(m+1.0g) ③(m+1.2g) ④(m+1.6g) ⑤(m+1.4g)
| A. | ①②④ | B. | ①⑤ | C. | ③④ | D. | ①②③④⑤ |
3.下列关于溶液和胶体的说法正确的是( )
| A. | 可以利用电泳现象区分溶液和胶体 | |
| B. | 可以利用胶体的丁达尔效应区分溶液和胶体 | |
| C. | 可以用过滤的方法分离溶液和胶体 | |
| D. | 溶液呈电中性,胶体是带电的 |
10.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系正确的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊,继续通入CO2至过量,溶液变澄清 | BaCl2溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色退去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,无明显变化 | Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.下列变化不能通过一步反应直接完成的是( )
| A. | Al→AlO2- | B. | CO2→HCO3- | C. | SiO2→H2SiO3 | D. | SO2→H2SO3 |
8.如图所示装置是一种可充电电池示意图,装置中的离子交换膜只允许Na+通过.已知充放电的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr.下列说法正确的是( )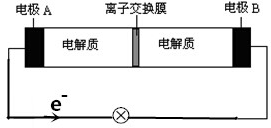

| A. | 放电时,Na+从右到左通过离子交换膜 | |
| B. | 放电时,负极反应式为3NaBr-2e-═NaBr3+2Na+ | |
| C. | 充电时,A极应与直流电源负极相连 | |
| D. | 放电时,当有0.1molNa+通过离子交换膜时,B极上有0.3molNaBr产生 |
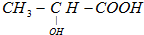 ),乳酸在微生物作用下分解为CO2和H2O.
),乳酸在微生物作用下分解为CO2和H2O.


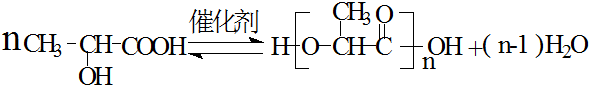 .
.