题目内容
14.乙烯是重要的有机化工原料.(1)实验室中,乙烯可由乙醇脱水制得.工业上,乙烯的获取主要来自于石油的裂解.
(2)将乙烯通入溴水中,可以观察到溴水褪色,请写出反应的化学方程式并注明反应类型:CH2=CH2+Br2→CH2BrCH2Br,反应类型为加成反应.
(3)下列物质与乙烯催化加氢得到的产物互为同系物的是C(选填编号).
a.C2H6 b.C3H6 c.C3H8 d.C4H8.
分析 (1)裂解得到不饱和烃,乙烯是石油裂解后的产物;
(2)乙烯中的官能团为碳碳双键,能够和溴加成反应;
(3)根据烷烃的同系物来解答,结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物.
解答 解:(1)石油的裂解是采用较高的温度,让大分子烃类有机物成为小分子烃的过程,裂解得到不饱和烃,乙烯是石油裂解后的产物,
故答案为:裂解;
(2)乙烯中的官能团为碳碳双键,能够和溴加成,故将乙烯通入溴水中,观察到的现象是溴的红棕色褪去,碳碳双键变单键,断键处加上加成溴原子,方程式为Br2+CH2=CH2→BrCH2-CH2Br,
故答案为:CH2=CH2+Br2→CH2BrCH2Br; 加成反应;
(3)乙烯和氢气的加成产物乙烷,C3H8与乙烷是同系物.
故答案为:C.
点评 本题主要考查了乙烯的结构与性质,题目难度不大,根据所学知识即可完成,平时注意基础知识的积累.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
4.一些烷烃的燃烧热(kJ•mol-1)如表:
下列表达正确的是( )
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A. | 热稳定性:正丁烷>异丁烷 | |
| B. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)→4CO2(g)+6H2O(g)△H=-1560.8kJ•mol-1 | |
| C. | 正戊烷的燃烧热大约在3540kJ•mol-1左右 | |
| D. | 相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
2.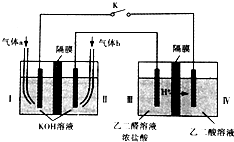 乙醛酸(HOOC-CHO)是有机合成的重要中间体.某同学组装了下图所示的电化学装置,电极材料Ⅰ~Ⅳ均为石墨,左池为氢氧燃料电池,右池为用“双极室成对电解法”生产乙醛酸,关闭K后,两极室均可产生乙醛酸,其中乙二醛与Ⅲ电极的产物反应生成乙醛酸.下列说法不正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.某同学组装了下图所示的电化学装置,电极材料Ⅰ~Ⅳ均为石墨,左池为氢氧燃料电池,右池为用“双极室成对电解法”生产乙醛酸,关闭K后,两极室均可产生乙醛酸,其中乙二醛与Ⅲ电极的产物反应生成乙醛酸.下列说法不正确的是( )
 乙醛酸(HOOC-CHO)是有机合成的重要中间体.某同学组装了下图所示的电化学装置,电极材料Ⅰ~Ⅳ均为石墨,左池为氢氧燃料电池,右池为用“双极室成对电解法”生产乙醛酸,关闭K后,两极室均可产生乙醛酸,其中乙二醛与Ⅲ电极的产物反应生成乙醛酸.下列说法不正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.某同学组装了下图所示的电化学装置,电极材料Ⅰ~Ⅳ均为石墨,左池为氢氧燃料电池,右池为用“双极室成对电解法”生产乙醛酸,关闭K后,两极室均可产生乙醛酸,其中乙二醛与Ⅲ电极的产物反应生成乙醛酸.下列说法不正确的是( )| A. | 电极Ⅱ上的电极反应式:O2+4e-+2H2O═4OH- | |
| B. | 电极Ⅳ上的电极反应式:HOOC-COOH+2e-+2H+═HOOC-CHO+H2O | |
| C. | 乙二醛与Ⅲ电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O=2HCl+HOOC-CHO | |
| D. | 若有2 mol H+ 通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol |
9.下列有关化学用语使用不正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | N2的结构式:N≡N | ||
| C. | Na的原子结构示意图: | D. | CH4分子的比例模型: |
19.元素周期律知识同族元素所形成的同一类型的化合物,其结构和性质都相似.化合物PH4I是一种白色晶体,下列对它的描述中不正确的是( )
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物可以分解为PH3和HI或H2和I2 | |
| C. | 这种化合物能跟碱反应 | |
| D. | 该化合物可以由PH3和HI化合而成 |
6.下列对各不等量关系的判断,其中正确的是( )
| A. | 相等物质的量的物质燃烧所消耗O2的量:环已烷>苯>苯甲酸 | |
| B. | 密度:CCl4>H2O>乙酸乙酯 | |
| C. | 相等质量的物质燃烧所消耗O2的量:乙炔>乙烯>乙烷 | |
| D. | 熔点:戊烷>2,2-二甲基戊烷>2,3-二甲基丁烷 |
3.下列说法中正确的是( )
| A. | 周期表中所有的族都是由长、短周期的元素共同组成 | |
| B. | 最外层电子数相同的元素不一定都是同一族 | |
| C. | 非金属元素都是主族元素,金属元素都是副族元素 | |
| D. | 元素周期表中共有18个纵行,每个纵行都是一个族,共有18个族 |
4.在锌与某浓度的盐酸反应的实验中,实验员得到下面的结果:
(1)写出实验中发生反应的离子方程式:Zn+2H+=Zn2++H2↑,该反应是放热反应(填“放热”或“吸热”);
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸花的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
(2)仔细观察A~F的实验数据对比,你可以得到关于温度影响反应速率结论,用此结论,计算:55℃时,2g锌薄片溶解于酸中需花12.5 s.
(3)对比结果B与F,解释结果F那么快的原因:B中锌是块状,F中锌是粉末状,粉末状时锌与酸溶液的接触面要比块状时的接触面大得多.
