题目内容
已知C(金刚石,S)?C(石墨,S);△H=-1.89kJ/mol C(金刚石,S)+O2(g)=CO2(g);△H=-akJ/mol C(石墨,S)+O2(g)=CO2(g);△H=-bkJ/mol,根据上述反应事实所得出的正确结论是( )
| A、a>b | B、a<b |
| C、a=b | D、金刚石比石墨稳定 |
考点:反应热的大小比较
专题:
分析:①C(金刚石、s)+O2(g)=CO2(g);△H=-akJ/mol,
②C(石墨、s)+O2(g)=CO2(g);△H=-bkJ/mol,
依据盖斯定律①-②得到C(金刚石、s)=C(石墨、s)△H=(b-a)KJ/mol=-1.89kJ/mol;物质能量越高越不稳定.
②C(石墨、s)+O2(g)=CO2(g);△H=-bkJ/mol,
依据盖斯定律①-②得到C(金刚石、s)=C(石墨、s)△H=(b-a)KJ/mol=-1.89kJ/mol;物质能量越高越不稳定.
解答:
解:①C(金刚石、s)+O2(g)=CO2(g);△H=-akJ/mol,
②C(石墨、s)+O2(g)=CO2(g);△H=-bkJ/mol,
由盖斯定律①-②得到C(金刚石、s)=C(石墨、s)△H=(b-a)KJ/mol=-1.89kJ/mol<0,所以a>b;
石墨的能量低于金刚石的能量,物质能量越高越不稳定,所以石墨更稳定,
故选A.
②C(石墨、s)+O2(g)=CO2(g);△H=-bkJ/mol,
由盖斯定律①-②得到C(金刚石、s)=C(石墨、s)△H=(b-a)KJ/mol=-1.89kJ/mol<0,所以a>b;
石墨的能量低于金刚石的能量,物质能量越高越不稳定,所以石墨更稳定,
故选A.
点评:本题考查了热化学方程式和盖斯定律的分析计算应用、物质稳定性与能量的关系等,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
下列叙述中,能证明某物质是弱电解质的是( )
| A、熔化时不能导电 |
| B、不是离子化合物是共价化合物 |
| C、水溶液的导电能力很差 |
| D、溶液中存在电离平衡,电离出的离子和未电离的分子共存 |
短周期元素X、Y、Z、W,它们的原子序数依次增大.X与Z同主族,并且原子序数之和为20.Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个.下列叙述正确的是( )
| A、原子半径Z>W>Y>X |
| B、Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应 |
| C、气态氢化物的稳定性Z>W |
| D、W的气态氢化物的化学式为H2W |
下列说法正确的是( )
| A、用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、粗铜精炼时,与电源正极相连的是纯铜 |
| D、钢铁发生电化腐蚀的负极反应式:Fe-3e-═Fe3+ |
X、Y是同一周期的两种主族元素,它们可能组成XY2型共价化合物,X、Y元素在周期表中的原子序数可能是( )
| A、6、8 | B、11、17 |
| C、11、16 | D、12、17 |
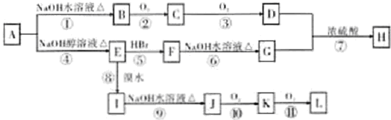
 (R为烃基)
(R为烃基) ③白磷 ④18O ⑤
③白磷 ④18O ⑤ ⑥红磷 ⑦16O ⑧氯气 ⑨H2O ⑩D2O
⑥红磷 ⑦16O ⑧氯气 ⑨H2O ⑩D2O ,写出酒精的同分异构体二甲醚的结构式
,写出酒精的同分异构体二甲醚的结构式