题目内容
保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处.pH< 的雨水称为酸雨;向煤中加入适量的 (填化学式),可以大大减少燃物产物中SO2的量.
考点:常见的生活环境的污染及治理
专题:化学应用
分析:正常的雨水常呈微酸性,这是由于在雨水中溶解了二氧化碳.通常所说的酸雨是指pH<5.6的雨水,酸雨主要是由化石燃料燃烧产生的二氧化硫、二氧化氮等酸性气体,经过复杂的大气化学反应,被雨水吸收溶解而成,向煤中加入适量的CaCO3(或CaO),可以大大减少燃物产物中SO2的量.
解答:
解:空气中含有二氧化碳,二氧化碳能和雨水反应生成碳酸,碳酸显酸性,所以正常的雨水常呈微酸性,pH约为5.6;而二氧化硫、氮氧化物是形成酸雨的重要物质,其溶液的pH<5.6,会形成酸雨;向煤中加入适量的CaCO3(或CaO),高温下石灰石分解生成CaO,可与SO2以及氧气反应生成硫酸钙,发生的反应为:2CaCO3+2SO2+O2
2CO2+2CaSO4,可以大大减少燃物产物中SO2的量,
故答案为:5.6;CaCO3(或CaO);
| ||
故答案为:5.6;CaCO3(或CaO);
点评:本题考查了酸雨的范围及正常雨水的pH,了解酸雨的形成原因及酸性物质的化学性质是解决本题的关键,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
下列情况可能引起水污染的是( )
①农业生产农药、化肥使用不当;②海上油轮原油的泄漏;
③工业生产中废气、废液、废渣排放;④生活垃圾的任意堆放.
①农业生产农药、化肥使用不当;②海上油轮原油的泄漏;
③工业生产中废气、废液、废渣排放;④生活垃圾的任意堆放.
| A、只有①② | B、只有②③ |
| C、①②③ | D、①②③④ |
近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和不锈钢为电极,以KI溶液(加少量K2CrO4)为电解液在一定条件下电解,反应方程式为KI+3H2O
KIO3+3H2↑.下列有关说法正确的是( )
| 电解 |
| A、电解时,石墨作阴极,不锈钢作阳极 |
| B、电解液调节至强酸性比较合适 |
| C、电解过程中,I-向阴极移动氧化成IO3- |
| D、电解中每转移0.6mol电子,理论上可得到21.4g无水KIO3晶体 |
为迎接北京奥运,北京曾采用机动车按照单双号行驶的方案,该方案既保障了交通秩序,又大大减少了空气污染.汽车尾气中所含污染物除碳氢化合物、可吸入颗粒物、一氧化碳外,还主要含有( )
| A、氮气 | B、硫化氢 |
| C、二氧化硫 | D、氮的氧化物 |
人们日益重视环境问题,下列说法不正确的是( )
| A、装饰装修材料中的甲醛、芳香烃及放射性物质都会造成室内污染 |
| B、人类超量碳排放及氮氧化物和二氧化硫的排放是形成酸雨的主要原因 |
| C、煤燃烧时加入少量的石灰石可以减少废气中的二氧化硫排放 |
| D、我国自实施“限塑令”以来,“白色污染”在一定程度上得到有效遏制 |
下列反应,①符合图象描述特点,②对其进行分析,结论是正确的.则合理选项为( )
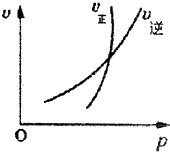

| A、2NO2(g)?N2O4(g);平衡后增大压强,气体颜色先变深后变浅 |
| B、N2(g)+3H2(g)?2NH3(g);将氨气液化分离后,有利于加快正反应速率 |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g);加大氧气浓度,能提高氨气平衡转化率 |
| D、2HI(g)?H2(g)+I2(g);平衡后又充入一定量HI,再次平衡时HI的转化率不变 |
 (1)表中A的数值为
(1)表中A的数值为