题目内容
铁、镁、铝3种金属,分别和同体积同浓度的盐酸反应,同温同压下,产生相同体积的氢气,则参加反应的金属( )
| A、所失去的电子数比是3:3:2 |
| B、质量相等 |
| C、物质的量相等 |
| D、质量比是28:12:9 |
考点:常见金属元素的单质及其化合物的综合应用,化学方程式的有关计算
专题:几种重要的金属及其化合物
分析:A.铁、镁、铝三种金属分别和等体积等浓度的盐酸反应,反应的本质都是金属失去电子;
B.同温同压下,产生相同体积的氢气,说明产生的氢气的物质的量相等,1mol铁失去2mol电子,1mol镁失去2mol电子,1mol铝失去3mol电子;
C.根据1mol铁失去2mol电子,1mol镁失去2mol电子,1mol铝失去3mol电子进行解答;
D.根据B分析进行解答;
B.同温同压下,产生相同体积的氢气,说明产生的氢气的物质的量相等,1mol铁失去2mol电子,1mol镁失去2mol电子,1mol铝失去3mol电子;
C.根据1mol铁失去2mol电子,1mol镁失去2mol电子,1mol铝失去3mol电子进行解答;
D.根据B分析进行解答;
解答:
解:A.铁、镁、铝三种金属分别和等体积等浓度的盐酸反应,反应的本质都是金属失去电子,溶液中氢离子得到电子变为氢气,故同温同压下,产生相同体积的氢气时,氢离子得到电子的数目必然相等,而这些电子均由金属提供,则参加反应的金属失去的电子数相等,故A错误;
B.铁、镁、铝三种金属,分别与同体积同浓度的盐酸反应后,同温同压下,产生相同体积的氢气,设所需要的金属质量分别是x、y、z,则有
×2=
×2=
×3,所以可得参加反应的金属质量比是28:12:9,故B错误;
C.若相同条件下产生相同体积的氢气,设为1mol,则根据反应的关系式可知:所需Fe、Mg、Al 三种金属的物质的量之比为:1mol:1mol:
mol=3:3:2,故C错误;
D.由B可知参加反应的金属质量比是28:12:9,故D正确;
故选D.
B.铁、镁、铝三种金属,分别与同体积同浓度的盐酸反应后,同温同压下,产生相同体积的氢气,设所需要的金属质量分别是x、y、z,则有
| x |
| 56 |
| y |
| 24 |
| z |
| 27 |
C.若相同条件下产生相同体积的氢气,设为1mol,则根据反应的关系式可知:所需Fe、Mg、Al 三种金属的物质的量之比为:1mol:1mol:
| 2 |
| 3 |
D.由B可知参加反应的金属质量比是28:12:9,故D正确;
故选D.
点评:本题主要考查了金属的化学性质以及金属与酸反应的实质和有关的计算,题目难度中等.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、8.4g NaHCO3固体中含有0.1NA个CO32- |
| B、1 mol CH3Cl中所含的共价键数为4NA |
| C、常温常压下,22.4L的NO2和CO2混合气体含有2NA个O原子 |
| D、5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |
某一种有机物的结构为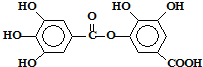 ,关于它的性质的叙述中不正确的是( )
,关于它的性质的叙述中不正确的是( )
 ,关于它的性质的叙述中不正确的是( )
,关于它的性质的叙述中不正确的是( )| A、它可以水解,水解产物只有一种 |
| B、1mol该有机物最多能和8molNaOH反应 |
| C、1mol该有机物最多能和4molBr2发生反应 |
| D、1mol该有机物最多能和8molH2发生加成反应 |
下列有机物的命名正确的是( )
| A、3,3-二甲基丁烷 |
| B、3-甲基-2-丁烯 |
| C、2-乙基丁烷 |
| D、2,3,5-三甲基己烷 |
铝投入到下列溶液中有气体生成,其中一定能大量共存的离子组是( )
| A、Ba2+、Na+、NO3-、Cl- |
| B、NH4+、K+、CH3COO-、SO42- |
| C、Ca2+、Br-、SO42-、Al3+ |
| D、Fe2+、OH-、MnO4-、Mg2+ |
下列金属在一定条件下能够与水反应,且生成金属氧化物的是( )
| A、K | B、Mg | C、Fe | D、Cu |
 下列实验操作或描述中正确的是( )
下列实验操作或描述中正确的是( )