题目内容
18.下列关于烃的性质描述中正确的是( )| A. | 实验室可用H2除去乙烷中的乙烯 | |
| B. | 在催化剂作用下,苯与溴水反应生成溴苯,发生了反应 | |
| C. | 乙烯结构中含有碳碳双键,苯中不含碳碳双键,但二者均可发生加成反应 | |
| D. | C2H6与Cl2发生取代反应,C2H4与HCl发生加成反应,均可得到纯净的C2H5Cl |
分析 A.乙烷中易引入新杂质氢气;
B.苯与溴水不反应;
C.乙烯与苯均可发生加成反应;
D.C2H6与Cl2发生取代反应,为连锁反应,产物复杂.
解答 解:A.乙烷中易引入新杂质氢气,不能除杂,应选溴水、洗气除杂,故A错误;
B.苯与溴水不反应,应选苯、液溴制备溴苯,故B错误;
C.乙烯与苯均可发生加成反应,如二者均与氢气发生加成反应,故C正确;
D.C2H6与Cl2发生取代反应,为连锁反应,产物复杂,而C2H4与HCl发生加成反可得到纯净的C2H5Cl,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机物的制备实验为解答的关键,侧重分析与应用能力的考查,注意性质及应用,题目难度不大.

练习册系列答案
相关题目
9.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | 原子核内有10个中子的氧原子818O | B. | 乙烯的结构简式为:C2H4 | ||
| C. | CH4分子的比例模型: | D. | -CH3(甲基)的电子式为: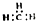 |
6.能正确表示下列反应的离子方程式的是( )
| A. | FeBr2溶液中通入少量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 铜溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
3.活性炭可处理大气污染物NO.T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
(1)2min内,用NO表示该反应的平均速率v(NO)=0.03mol•L-1•min-1.
(2)该反应的化学方程式是C+2NO?N2+CO2.
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是②④.
①v(NO):v(A):v(B)=2:1:1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
 (4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
①a处通入的物质是CH3OH,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;
②b处电极反应式为3O2+12e-+12H+=6H2O;
③电池工作时H+由负极移向正极(填正、负极).
| 活性炭/mol | NO/mol | A/mol | B/mol | |
| 起始状态 | 2.030 | 0.100 | 0 | 0 |
| 2min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(2)该反应的化学方程式是C+2NO?N2+CO2.
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是②④.
①v(NO):v(A):v(B)=2:1:1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
 (4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.①a处通入的物质是CH3OH,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;
②b处电极反应式为3O2+12e-+12H+=6H2O;
③电池工作时H+由负极移向正极(填正、负极).
10.用括号内的试剂和分离方法,除去下列物质中的少量杂质,正确的是( )
| A. | 乙醇中的水(生石灰,蒸馏) | B. | 乙烷中的乙烯(酸性KMnO4溶液,洗气) | ||
| C. | 溴苯中的溴(KI溶液,分液) | D. | 乙酸乙酯中的乙酸(NaOH溶液,蒸馏) |