题目内容
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,5.6L氯气和16.8L氧气的混合气体中含有分子数为NA |
| B、标准状况下,22.4LH2O所含有原子数为3NA |
| C、NA个N2分子所占的体积与0.5 NA个H2分子所占的体积比一定是2:1 |
| D、常温下,2.3g Na完全与O2反应失去的电子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据N=
NA来计算分子数;
B、标况下,水为液态;
C、气体的体积与温度和压强有关.
D、依据n=
计算物质的量,结合钠原子结构计算是电子数.
| V |
| Vm |
B、标况下,水为液态;
C、气体的体积与温度和压强有关.
D、依据n=
| m |
| M |
解答:
解:A、氯气和氧气不反应,标况下,5.6L氯气和16.8L氧气的混合气体的物质的量是1mol,所以含有的分子数为NA,故A正确;
B、标况下,水为液态,故B错误;
C、气体的体积与温度和压强有关,未标明温度和压强,所以气体摩尔体积未知导致气体体积无法计算,故C错误;
D、2.3g金属钠物质的量为0.1mol,与氧气反应后变为+1价,故失去的电子数为0.1NA,故D错误;
故选A.
B、标况下,水为液态,故B错误;
C、气体的体积与温度和压强有关,未标明温度和压强,所以气体摩尔体积未知导致气体体积无法计算,故C错误;
D、2.3g金属钠物质的量为0.1mol,与氧气反应后变为+1价,故失去的电子数为0.1NA,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列各组离子,能在溶液中大量共存的是( )
| A、Na+、Al3+、AlO2-、Br- |
| B、H+、Fe2+、SO42-、NO3- |
| C、K+、NH4+、CO32-、OH- |
| D、Ca2+、Al3+、NO3-、Cl- |
未来新能源的特点是资源丰富,可以再生,在使用过程中对环境无污染或污染很小.下列符合未来新能源标准的是:
①天然气 ②风能 ③石油 ④太阳能 ⑤生物质能 ⑥煤 ⑦氢能( )
①天然气 ②风能 ③石油 ④太阳能 ⑤生物质能 ⑥煤 ⑦氢能( )
| A、①④⑥⑦ | B、②④⑤⑦ |
| C、①②③⑥ | D、②④⑤⑥ |
用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A、标准状况下,22.4LH2含有的分子数为1 NA |
| B、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C、通常状况下,1 NA个 CO2分子占有的体积为22.4L |
| D、1L0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
下列离子方程式正确的是( )
| A、用醋酸除水垢:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- | ||
B、氯乙酸与氢氧化钠溶液共热:ClCH2COOH+OH-
| ||
C、乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2+OH-
| ||
D、服用阿司匹林过量出现水杨酸(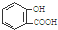 )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: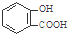 +2 HCO3-→ +2 HCO3-→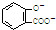 +2 CO2↑+2 H2O +2 CO2↑+2 H2O |
分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A、NaHCO3和Na2O都属于钠盐 |
| B、K2O和Na2SiO3都属于氧化物 |
| C、KOH和Na2CO3都属于强碱 |
| D、H2SO4和HNO3都属于酸 |
由相同条件下的三个反应:①2NaA+B2=2NaB+A2; ②2NaC+A2=2NaA+C2;③2NaB+D2=2NaD+B2;可判断( )
| A、氧化性:A2>B2>C2>D2 |
| B、还原性:C->A->B->D- |
| C、2NaD+A2=2NaA+D2可进行 |
| D、2NaC+B2=2NaB+C2不能进行 |