题目内容
已知氯化铝的熔点为190℃(2.02×105Pa),但它在180℃即开始升华.在500K和1.01×105Pa时,它的蒸气密度(换算为标准状况)为11.92g/L.有关氯化铝的叙述中错误的是( )A.氯化铝是共价化合物
B.氯化铝的化学式应为Al2Cl6
C.氯化铝的结构式为:
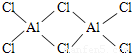 ,分子结构中有配位键
,分子结构中有配位键D.在一定条件下,将AlCl3晶体加热至融化,熔融态的AlCl3可以导电
【答案】分析:由于AlCl3的熔点较低,且易升华,因此为共价化合物,是分子晶体,500 K和1.01×105 Pa时,M=11.92 g?L-1×22.4 L?mol-1=267 g?mol-1,其化学式为Al2Cl6,共价化合物在熔融状态下不导电.
解答:解:A.根据氯化铝熔点低及在180℃时开始升华,判断其为共价化合物,故A正确;
B.500 K和1.01×105 Pa时,M=11.92 g?L-1×22.4 L?mol-1=267 g?mol-1,其化学式为Al2Cl6,故B正确;
C.氯化铝的化学式应为Al2Cl6,分子中Al可提供空轨道,Cl可提供孤电子对,可形成配位键,故C正确;
D.氯化铝是共价化合物,在熔融状态下不导电,故D错误.
故选D.
点评:本题考查配合物知识,题目难度不大,注意根据晶体的物理性质判断晶体类型,为解答该题的关键.
解答:解:A.根据氯化铝熔点低及在180℃时开始升华,判断其为共价化合物,故A正确;
B.500 K和1.01×105 Pa时,M=11.92 g?L-1×22.4 L?mol-1=267 g?mol-1,其化学式为Al2Cl6,故B正确;
C.氯化铝的化学式应为Al2Cl6,分子中Al可提供空轨道,Cl可提供孤电子对,可形成配位键,故C正确;
D.氯化铝是共价化合物,在熔融状态下不导电,故D错误.
故选D.
点评:本题考查配合物知识,题目难度不大,注意根据晶体的物理性质判断晶体类型,为解答该题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
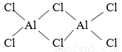 ,分子结构中有配位键
,分子结构中有配位键