题目内容
9.可逆反应A(g)+3B(g)?2C(g)+2D(g),在四种不同情况下的反应速率分别如下,其中反应速率最大的是( )| A. | VA=0.15 mol•L-1•min-1 | B. | VB=0.6 mol•L-1•min-1 | ||
| C. | VC=0.4 mol•L-1•min-1 | D. | VD=0.1 mol•L-1•min-1 |
分析 反应速率的单位相同,用各物质表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
解答 解:A、v(A)/1=0.15mol/(L•min),
B、v(B)/3=0.2mol/(L•min),
C、v(C)/2=0.2mol/(L•min),
D、v(D)/2=0.05mol/(L•min),
所以反应速率v(B)=v(C)>v(A)>v(D).
故选BC.
点评 比较反应速率常用的两种方法:(1)归一法:将同一反应中的不同物质的反应速率转化成同一物质的反应速率,再较小比较.(2)比值法:用各物质的量表示的反应速率除以对应各物质的化学计量数,数值大的反应速率快.
比较反应速率时注意(1)反应速率的单位要相同(2)单位时间内反应物或生成物的物质的量变化大,反应速率不一定快,反应速率是用单位时间内浓度的变化量来表示的.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫 | |
| B. | 二氧化碳和CaCl2溶液反应,生成白色沉淀 | |
| C. | 二氧化硅和烧碱溶液反应,使溶液的碱性一定减弱 | |
| D. | 在常温下,浓硫酸不与铜反应,是因为铜被钝化 |
20.下列关于电解质溶液的叙述正确的是( )
| A. | 在pH=3的溶液中,Na+、Cl-、Fe2+、ClO-可以大量共存 | |
| B. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| C. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3•H2O)增大 |
17.下列气体,能使紫色石蕊试剂先变红后褪色的是( )
| A. | CO2 | B. | 氯气 | C. | O3 | D. | SO2 |
18.下列反应中反应物总能量低于生成物总能量的是( )
| A. | 木炭的燃烧 | B. | 氢氧化钡晶体与氯化铵晶体混合 | ||
| C. | 镁条与稀硫酸的反应 | D. | 生石灰溶于水 |
19.下列各图所示的实验方法,装置或操作正确的是( )
| A. |  称量NaOH固体 | B. |  收集氯气 | C. |  加热蒸发溶液 | D. |  分离汽油和水 |
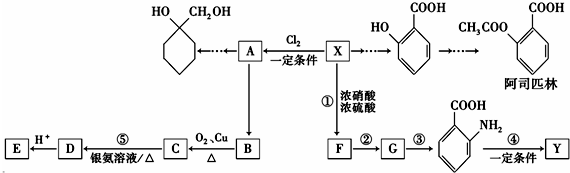

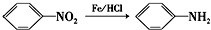 (苯胺,易被氧化)
(苯胺,易被氧化)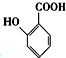 中官能团名称为酚羟基、羧基;
中官能团名称为酚羟基、羧基; ;
; $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$  +(n-1)H2O;
+(n-1)H2O; 的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2
的合成路线(无机试剂任用).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2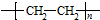
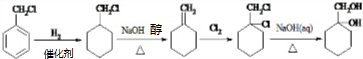 .
.