题目内容
将铜投入一定量的稀硝酸中,铜完全溶解后,测得反应后溶液中的Cu2+和NO3-的物质的量之比为3:7,则参加反应的HNO3和参加反应之前的HNO3量的物质的量之比为 .
考点:化学方程式的有关计算
专题:计算题
分析:反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,反应后溶液中的Cu2+和NO3-的物质的量之比为3:7,根据铜离子求出参加反应的NO3-,再求参加反应的HNO3和参加反应之前的HNO3量的物质的量之比.
解答:
解:反应的离子方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,反应后溶液中的Cu2+和NO3-的物质的量之比为3:7,
设反应的铜离子为3mol,则溶液中剩余的NO3-为7mol,
由方程式中的关系可知,反应消耗的NO3-为2mol,
所以反应前HNO3为2+7=9mol,
所以参加反应的HNO3和参加反应之前的HNO3量的物质的量之比为2:9,
故答案为:2:9.
设反应的铜离子为3mol,则溶液中剩余的NO3-为7mol,
由方程式中的关系可知,反应消耗的NO3-为2mol,
所以反应前HNO3为2+7=9mol,
所以参加反应的HNO3和参加反应之前的HNO3量的物质的量之比为2:9,
故答案为:2:9.
点评:本题考查硝酸的性质和有关方程式的计算,侧重于学生的分析能力和计算能力的考查,题目难度不大,注意结合反应的化学方程式从质量守恒的角度解答该题.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
某烷烃一个分子里含有9个碳原子,其一氯代物只有两种,这种烷烃的名称是( )
| A、正壬烷 |
| B、2,6二甲基庚烷 |
| C、2,3,4三甲基己烷 |
| D、2,2,4,4四甲基戊烷 |
反应N2(g)+O2(g)?2NO(g)在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是( )
| A、平衡向逆反应方向移动,N2和O2的转化率都减小 |
| B、平衡向正反应方向移动,N2和O2的转化率都增大 |
| C、压强增大平衡不移动,N2的转化率不变 |
| D、平衡向正反应方向移动,N2的转化率减小,O2的转化率增大 |
可逆反应:3R(气)?3M(?)十N(?) ( 吸热反应 ),随着温度的升高,气体平均相对分子质量有变小的趋势.则下列判断中正确的是( )
| A、M和N可能都是固体 |
| B、若N为固体.则M一定是气体 |
| C、M和N一定都是气体 |
| D、若M为固体.则N一定是气体 |
20mL0.1mol/L醋酸与40mL0.05mol/L氢氧化钠溶液混合,在所得溶液中( )
| A、c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、c(Na+)>c(CH3COO-)>c(H+)=c(OH-) |
| D、c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1mol氢气的化学键消耗的能量为Q1kJ,破坏1mol氯气的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ,下列关系式正确的是( )
| A、Q1+Q 3 |
| B、Q1+Q2>2Q3 |
| C、Q1+Q2<Q3 |
| D、Q1+Q2<2Q3 |
下列各装置中,不能构成原电池的是(电解质都为稀硫酸)( )
A、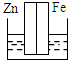 |
B、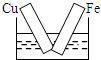 |
C、 |
D、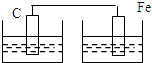 |
下列物质中,摩尔质量最大的是 ( )
| A、10mL H2O |
| B、0.1mol HCl |
| C、24g Mg |
| D、1g CaCO3 |
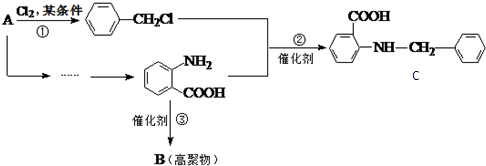

 中官能团的名称
中官能团的名称 多一个碳的同系物,则满足下列条件的D的同分异构体共有
多一个碳的同系物,则满足下列条件的D的同分异构体共有