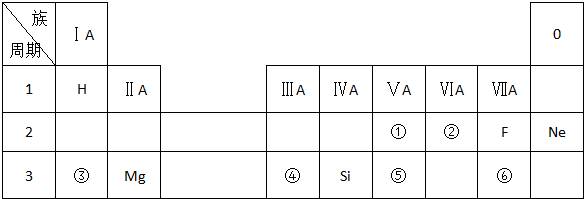
题目内容
有关能量的判断或表示方法正确的是( )
| A、由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.3 kJ |
| B、等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| C、从C(S、石墨)=C(S、金刚石)△H=+1.9kJ/mol,可知石墨比金刚石更稳定 |
| D、2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2 H2O(l)△H=-285.8kJ/mol |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A.乙酸是弱酸,电离过程是吸热过程;
B.硫固体转化为硫蒸气的过程是吸热该过程,硫的燃烧过程是放热过程;
C.物质具有的能量越低越稳定;
D.根据热化学方程式的意义和书写方法来判断.
B.硫固体转化为硫蒸气的过程是吸热该过程,硫的燃烧过程是放热过程;
C.物质具有的能量越低越稳定;
D.根据热化学方程式的意义和书写方法来判断.
解答:
解:A.乙酸是弱酸,电离过程是吸热过程,含1mol CH3COOH的溶液与含1mol NaOH的稀溶液混合,放出热量小于57.3 kJ,故A错误;
B.硫固体转化为硫蒸气的过程是吸热该过程,硫蒸气和硫固体分别完全燃烧,硫蒸气放出热量更多,故B错误;
C.从C(石墨)═C(金刚石)△H=+1.9kJ/mol,可知石墨具有的能量较低,物质具有的能量越低越稳定,所以石墨比金刚石更稳定,故C正确;
D.2gH2即1molH2完全燃烧生成液态水放出285.8kJ热量,则2molH2燃烧放出的热量285.8kJ×2=571.6KJ,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2 H2O(l)△H=-571.6kJ/mol,故D错误;
故选C.
B.硫固体转化为硫蒸气的过程是吸热该过程,硫蒸气和硫固体分别完全燃烧,硫蒸气放出热量更多,故B错误;
C.从C(石墨)═C(金刚石)△H=+1.9kJ/mol,可知石墨具有的能量较低,物质具有的能量越低越稳定,所以石墨比金刚石更稳定,故C正确;
D.2gH2即1molH2完全燃烧生成液态水放出285.8kJ热量,则2molH2燃烧放出的热量285.8kJ×2=571.6KJ,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2 H2O(l)△H=-571.6kJ/mol,故D错误;
故选C.
点评:本题考查化学反应的反应热和焓变间的关系知识,注意中和热的测定实验中使用的是强酸和强碱的稀溶液,题目难度不大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
在下列溶液中,能大量共存的离子组是( )
| A、能使pH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- | ||
B、常温下
| ||
| C、含有大量Fe3+的溶液中:SO42-、S2-、AlO2-、ClO- | ||
| D、能使石蕊试液显红色的溶液中:K+、SO42-、CH3COO-、PO43- |
下列物质能由单质直接化合而成,但不能由单质和盐酸反应生成的是( )
| A、FeCl2 |
| B、CuCl2 |
| C、AlCl3 |
| D、NaCl |
将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如图所示,最先观察到变为红色的区域为( )
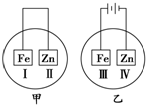

| A、Ⅰ和Ⅱ | B、Ⅰ和Ⅳ |
| C、Ⅱ和Ⅲ | D、Ⅱ和Ⅳ |
下列有关性质的比较中,大小顺序排列错误的是( )
| A、物质的熔点:石英>食盐>碘 |
| B、热稳定性:CH4>H2S>HCl>NH3 |
| C、下列元素的最高价氧化物的水化物酸碱性强弱:碱性:NaOH>Al(OH)3 酸性HClO4>H2SO4 |
| D、分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
向碘水中加入酒精,观察到的现象是( )
A、 |
B、 |
C、 |
D、 |
日常生活中遇到的很多问题都涉及到化学知识,下列有关叙述不正确的是( )
| A、用纯碱溶液洗涤餐具上的油污 |
| B、用食盐水清洗热水瓶中的水垢 |
| C、食盐中添加适量KIO3 |
| D、利用丁达尔效应区别蛋白质溶液和食盐溶液 |