题目内容
已知氮的氧化物和NaOH 溶液发生的化学反应如下:3NO2+2NaOH=2NaNO3+NO↑+H2O NO2+NO+2NaOH=2NaNO2+H2O
现有m mol NO2 和 n mol NO 组成的混合气体,用VLNaOH 溶液恰好使其完全吸收无气体剩余,则此NaOH溶液浓度为( )
现有m mol NO2 和 n mol NO 组成的混合气体,用VLNaOH 溶液恰好使其完全吸收无气体剩余,则此NaOH溶液浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:化学方程式的有关计算
专题:计算题
分析:NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,反应生成物有NaNO3、NaNO2,由化学式可知n(Na原子)=n(N原子),根据原子守恒计算n(NaOH),再根据c=
计算NaOH的物质的量浓度.
| n |
| V |
解答:
解:反应生成物有NaNO3、NaNO2,由化学式可知n(Na原子)=n(N原子),由于恰好反应,根据原子守恒可知n(NaOH)=n(NO)+n(NO2)=(m+n)mol,
故此氢氧化钠溶液的物质的量浓度
=
mol?L-1,
故选D.
故此氢氧化钠溶液的物质的量浓度
| (m+n)mol |
| VL |
| m+n |
| V |
故选D.
点评:本题考查混合物的有关计算,难度中等,根据原子守恒计算是关键,侧重对解题方法技巧与学生思维能力的考查.

练习册系列答案
相关题目
新的替代能源主要包括( )
①核能 ②柴草 ③焦炭 ④太阳能 ⑤氢能 ⑥液化气 ⑦水煤气 ⑧天然气.
①核能 ②柴草 ③焦炭 ④太阳能 ⑤氢能 ⑥液化气 ⑦水煤气 ⑧天然气.
| A、①④⑤ | B、②③⑥⑦ |
| C、①④⑤⑦ | D、①④⑤⑥ |
下列物质能发生催化氧化且产物是2甲基丁醛的是( )
A、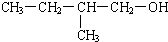 |
B、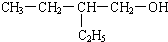 |
C、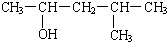 |
D、 |
下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是( )
| A、Cu与浓硝酸反应比稀硝酸反应快 |
| B、Cu能与浓硝酸反应,而不与浓盐酸反应 |
| C、N2与O2在常温、常压下不反应,放电时可反应 |
| D、Cu与浓硫酸能反应,而不与稀硫酸反应 |
金属钠久置于空气中,最后变为( )
| A、Na2O |
| B、Na2CO3 |
| C、NaOH |
| D、Na2CO3?10H2O |
向纯水中加入少量NaHSO4晶体,若温度不变,则溶液中( )
| A、水电离出的H+大于水电离出的OH-浓度 |
| B、c(H+).c(OH-)乘积增大 |
| C、酸性增强 |
| D、H+,OH-浓度均增大 |
有机化合物与人类生活水平的提高和人类社会的发展密不可分.下列对有机化合物的认识正确的是( )
| A、碳原子的成键方式多是有机物种类繁多原因之一 |
| B、有机化合物都含有碳、氢元素 |
| C、有机化合物都具有同分异构现象 |
| D、有机化合物都具有可燃性 |
对于某酸的酸式盐NaHY的水溶液的下列叙述中,正确的是( )
| A、该酸式盐的水溶液一定显酸性 |
| B、该酸式盐的水溶液一定呈碱性 |
| C、若HY-能水解,水解方程式为HY-+H2O?Y2-+H3O+ |
| D、若HY-能水解,水解方程式为HY-+H2O?H2Y+OH- |