题目内容
 NH4Al(SO4)2是加工食品最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业有广泛应用.试回答下列问题:
NH4Al(SO4)2是加工食品最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业有广泛应用.试回答下列问题:(1)NH4Al(SO4)2可用做净水剂,其理由是
(2)相同条件下,浓度相同的NH4Al(SO4)2溶液和NH4HSO4溶液中,NH4+浓度较大的是
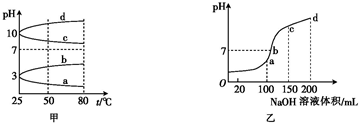
(3)图甲是0.1mol?L-1某电解质溶液的pH随温度变化的图象.
①其中符合0.1mol?L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
②25℃时,0.1mol?L-1NH4Al(SO4)2溶液中:2c(SO42-)-c(NH4+)-3c(Al3+)=
(4)室温时,向100mL 0.1mol?L-1NH4HSO4溶液中滴加0.1mol?L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图乙,试分析图中a、b、c、d四个点中,水的电离程度最大是
考点:镁、铝的重要化合物,弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:
分析:(1)Al3+水解生成的Al(OH)3具有吸附性;
(2)NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
②根据电荷守恒定律解题;
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离.
(2)NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
②根据电荷守恒定律解题;
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离.
解答:
解:(1)Al3+水解生成的Al(OH)3具有吸附性,离子方程式:Al3++3H2O?Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水,
故答案为:Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O?Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2与NH4HSO4中的NH4+均发生水解,但是NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解,因为HSO4-电离生成的H+浓度比Al3+水解生成的H+浓度大,所以NH4HSO4中NH4+水解程度比NH4Al(SO4)2中的小,则浓度相同的NH4Al(SO4)2溶液和NH4HSO4溶液中,NH4+浓度较大的是NH4HSO4溶液,故答案为:NH4HSO4溶液;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为a,故答案为:a;
②根据电荷守恒,可以求出2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol?L-1[c(OH-)太小,可忽略],故答案为:10-3 mol?L-1;
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离,所以水的电离程度最大是a点,故答案为:a.
故答案为:Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O?Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2与NH4HSO4中的NH4+均发生水解,但是NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解,因为HSO4-电离生成的H+浓度比Al3+水解生成的H+浓度大,所以NH4HSO4中NH4+水解程度比NH4Al(SO4)2中的小,则浓度相同的NH4Al(SO4)2溶液和NH4HSO4溶液中,NH4+浓度较大的是NH4HSO4溶液,故答案为:NH4HSO4溶液;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为a,故答案为:a;
②根据电荷守恒,可以求出2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol?L-1[c(OH-)太小,可忽略],故答案为:10-3 mol?L-1;
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3?H2O,(NH4)2SO4可以促进水的电离,而NH3?H2O抑制水的电离,所以水的电离程度最大是a点,故答案为:a.
点评:本题考查盐类的水解和离子浓度大小的比较,题目难度较大,(3)②为易错点,注意根据守恒思想解题.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
实验室收集氯气,可供选择的方法有:①向上排空气法;②向下排空气法;③排饱和食盐水法;④排烧碱溶液法;⑤多余氯气通入水中;⑥多余氯气直接排入大气中;⑦多余氯气通入氢氧化钠溶液中;应选用的方法是( )
| A、①④⑤ | B、①③⑦ |
| C、②④⑥ | D、①③⑤ |
下列各组物质反应后,再滴入KSCN溶液,显红色的是( )
| A、过量铁与稀盐酸 |
| B、过量氯水与FeCl2溶液 |
| C、过量铁粉与CuCl2溶液 |
| D、过量铁粉与FeCl3溶液 |
钨酸盐在新材料的制造中有重要应用,一种钨酸盐的制备方式如下:2GeO(g)+W2O6(g)?2GeWO4(g)△H<0.下列说法中正确的是( )
| A、增大压强可提高GeWO4的产率 |
| B、增加GeO有利于提高GeO的转化率 |
| C、实际生产中为提高经济效益要尽可能地降低反应温度 |
| D、及时分离出GeWO4可增大正反应速率 |
已知有钠、钾及钠钾合金,对于它们三者熔点高低比较正确的是( )
| A、钠钾合金>钠>钾 |
| B、钠>钾>钠钾合金 |
| C、钠>钠钾合金>钾 |
| D、钾>钠钾合金>钠 |
当周围空间不慎有大量氯气溢出时,处在该环境中的人可以用浸有一定浓度某种物质的水溶液的毛巾捂住鼻子,以防中毒,最适宜采用的物质是( )
| A、NaOH |
| B、KI |
| C、NH3?H2O |
| D、Na2CO3 |
氧化钙是碱性氧化物,下列关于氧化钙性质叙述不正确的是( )
| A、氧化钙可以与水反应生成碱 |
| B、氧化钙可以与盐酸反应 |
| C、氧化钙可以和Na2O反应 |
| D、氧化钙可以与CO2反应 |