题目内容
氢元素有三种同位素,各有各的丰度.其中
H的丰度指的是( )
1 1 |
A、自然界
| ||
B、
| ||
C、自然界
| ||
D、
|
考点:同位素及其应用
专题:
分析:同位素在自然界中的丰度,又称天然存在比,指的是该同位素在这种元素的所有天然同位素中所占的比例.
解答:
解:同位素在自然界中的丰度,指的是该同位素在这种元素的所有天然同位素中所占的比例.故
H的丰度指的是自然界
H原子个数所占氢元素的百分数,
故选C.
1 1 |
1 1 |
故选C.
点评:本题考查同位素在自然界中的丰度,难度不大.掌握同位素在自然界中的丰度的定义是解题的关键.

练习册系列答案
相关题目
25℃时pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得混合液的pH=11,则NaOH溶液与H2SO4溶液的体积比是( )
| A、1:9 | B、1:11 |
| C、9:1 | D、11:1 |
关于元素周期律的叙述不正确的是( )
| A、同周期元素,从左到右电负性依次增大 |
| B、主族元素的最高化合价都等于最外层电子数(O、F除外) |
| C、同主族元素,从上到下,原子半径依次增大 |
| D、金属元素的正化合价越高,其对应的氢氧化物的碱性越强 |
下列说法中不正确的是( )
| A、1mol任何物质都约含有6.02×1023个原子 |
| B、0.012kg12C约含有6.02×1023个碳原子 |
| C、使用摩尔这一单位时必须指明微粒的种类或名称 |
| D、物质的量是国际单位制中七个基本物理量之一 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 |
| B、pH=2的CH3COOH和pH=12的NaOH溶液等体积混合 |
| C、CH3COONa溶液 |
| D、c(NH+4)=c(Cl-)的NH4Cl和氨水的混合溶液 |
下列说法不正确的是( )
| A、原电池是将化学能转化为电能的装置 |
| B、电镀过程相当于金属的“迁移”,可认为是物理变化 |
| C、不能自发进行的氧化还原反应通过电解的方法有可能实现 |
| D、从理论上说,任何一个可自发进行的氧化还原反应都可以设计成原电池反应 |
 (Ⅰ)在下面的装置中,A是Cl2发生装置,C、D为气体的净化装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置.
(Ⅰ)在下面的装置中,A是Cl2发生装置,C、D为气体的净化装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置.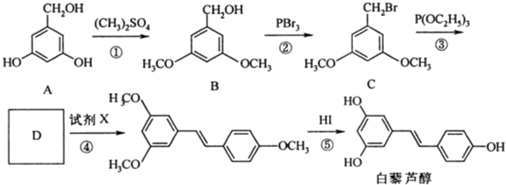
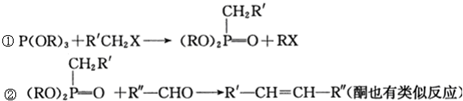
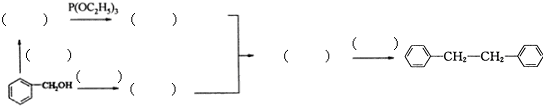
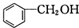 和P(OC2H5)3为原料,选择适当的无机试剂和催化剂,通过合理的途径合成
和P(OC2H5)3为原料,选择适当的无机试剂和催化剂,通过合理的途径合成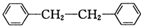 .请补全下列合成路线(含条件、试剂和主要产物的结构简式).
.请补全下列合成路线(含条件、试剂和主要产物的结构简式).