题目内容
10.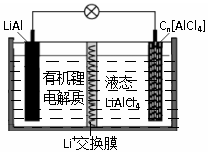 某种新型电池的工作原理如图”所示.Cn为石墨烯,液态LiAlCl4中含有Li+和AlCl4-.下列说法正确的是( )
某种新型电池的工作原理如图”所示.Cn为石墨烯,液态LiAlCl4中含有Li+和AlCl4-.下列说法正确的是( )| A. | 充电时,Cn为阳极,电极反应为:Cn+AlCl4--e-═Cn[AlCl4] | |
| B. | 放电时,当电路中通过0.1mol电子时,有0.1molLi+通过交换膜向LiAl极移动 | |
| C. | LiAl具有强氧化性,放电时作负极材料 | |
| D. | 电池中可能发生副反应:2Al+6H2O═2Al(OH)3+3H2↑,故该电池存在安全隐患 |
分析 A、充电时,在阳极上发生失电子的氧化反应,据此回答;
B、在原电池中,电解质里的阳离子移向正极,阴离子移向负极;
C、在原电池的负极上具有还原性的物质失电子;
D、金属铝和水之间不会发生反应.
解答 解:A、充电时,电解池的正极和原电池的正极相连,在阳极上发生失电子的氧化反应Cn+AlCl4--e-═Cn[AlCl4],故A正确;
B、在原电池中,电解质里的阳离子移向正极,阴离子移向负极,放电时,当电路中通过0.1mol电子时,有0.1molLi+通过交换膜向Cn[AlCl4]极移动,故B错误;
C、在原电池的负极上具有还原性的物质失电子,LiAl具有还原性,放电时作负极材料,故C错误;
D、金属铝和水之间不会发生反应,所以电池中不可能发生副反应:2Al+6H2O═2Al(OH)3+3H2↑,故D错误.
故选A.
点评 本题考查了原电池和电解池原理,根据元素化合价变化确定各个电极上发生的反应,难点是电极反应式的书写,题目难度中等.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
20.下列实验能达到目的是( )
| A. | 用KI溶液除去FeCl2溶液中的Fe3+ | B. | 用饱和NaHCO3溶液除去Cl2中的HC1 | ||
| C. | 用金属钠鉴别1一丁醇和2一丁醇 | D. | 用溴水鉴别苯和己烯 |
1.化合物乙是一种治疗神经类疾病的药物,可由化合物甲经多步反应得到.下列有关甲、乙的说法正确的是( )
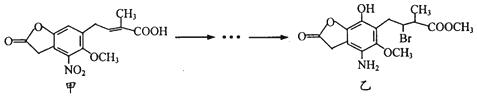

| A. | 甲的分子式为C14H14NO7 | |
| B. | 甲、乙中各有1个手性碳原子 | |
| C. | 可用NaHCO3溶液或FeCl3溶液鉴别化合物甲、乙 | |
| D. | 乙能与盐酸、NaOH溶液反应,且lmol乙最多能与4 mol NaOH反应 |
18.为探究元素性质递变规律,设计如下实验.
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选).
A.剧烈反应,迅速产生大量无色气体.
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色.
C.反应不十分剧烈;产生无色气体.
D.有气体产生,溶液变成浅红色.
(2)实验④:向1mL 1mol/L AlCl3溶液中滴加2mol/L NaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失.
请用离子方程式解释该实验现象:Al3++3OH-═Al(OH)3↓;、Al(OH)3+OH-═AlO2-+2H2O
(3)实验⑤:在试管中加入3~5mL Na2SiO3溶液,逐滴加入稀硫酸,边加边振荡.观察试管中出现白色凝胶.相应化学方程式:H2SO4+Na2SiO3═H2SiO3(胶体)+Na2SiO4,证明酸性:H2SO4>H2SiO3(用化学式表示).
(4)实验⑥:向新制得的Na2S溶液中滴加新制的氯水.观察试管中出现黄色沉淀.相应离子方程式:S2-+Cl2═S↓+2Cl-,证明氧化性:Cl2>S(用化学式表示).
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐减弱 (选填“增强”或“减弱”),硅、硫、氯的非金属性逐渐增强(选填“增强”或“减弱”).
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选).
| 实验序号 | 实验步骤 | 实验现象 |
| ① | 将一小块金属钠放入滴有酚酞溶液的冷水中. | B |
| ② | 将磨去表面氧化膜的一小段镁条放入试管中,加入2mL水,滴入2滴酚酞溶液,加热至水沸腾. | D |
| ③ | 将磨去表面氧化膜的一小段镁条投入2mL 1mol/L盐酸中. | A |
| ④ | 将磨去表面氧化膜的一小片铝投入2mL 1mol/L盐酸中. | C |
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色.
C.反应不十分剧烈;产生无色气体.
D.有气体产生,溶液变成浅红色.
(2)实验④:向1mL 1mol/L AlCl3溶液中滴加2mol/L NaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失.
请用离子方程式解释该实验现象:Al3++3OH-═Al(OH)3↓;、Al(OH)3+OH-═AlO2-+2H2O
(3)实验⑤:在试管中加入3~5mL Na2SiO3溶液,逐滴加入稀硫酸,边加边振荡.观察试管中出现白色凝胶.相应化学方程式:H2SO4+Na2SiO3═H2SiO3(胶体)+Na2SiO4,证明酸性:H2SO4>H2SiO3(用化学式表示).
(4)实验⑥:向新制得的Na2S溶液中滴加新制的氯水.观察试管中出现黄色沉淀.相应离子方程式:S2-+Cl2═S↓+2Cl-,证明氧化性:Cl2>S(用化学式表示).
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐减弱 (选填“增强”或“减弱”),硅、硫、氯的非金属性逐渐增强(选填“增强”或“减弱”).
5.下列说法中正确的是( )
| A. | 分子中键能越大,键长越长,则分子越稳定 | |
| B. | 乳酸分子[CH3-CH(OH)-COOH]中有 1 个手性碳且 1 mol 该分子中有 11 mol σ 键 | |
| C. | PCl5分子中P原子和Cl原子最外层都满足8电子结构 | |
| D. | H-O键键能为463 kJ/mol,即18 g H2O分解成H2和O2时,消耗能量为2×463 kJ |
15.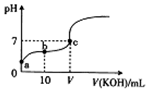 已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是 ( )
已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是 ( )
 已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是 ( )
已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是 ( )| A. | a点溶液中c(H+)为4.0×10-5mol/L | |
| B. | c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO-)>c(H+)=c(OH-) | |
| C. | V=20 | |
| D. | a、b、c三点中水的电离程度最大的是c点 |
2.已知热化学方程式:C(s,石墨)→C(s,金刚石)-3.9kJ.下列有关说法正确的是( )
| A. | 石墨和金刚石完全燃烧,后者放热多 | |
| B. | 金刚石比石墨稳定 | |
| C. | 等量的金刚石储存的能量比石墨高 | |
| D. | 石墨很容易转化为金刚石 |
12.用下列装置在实验室中进行二氧化硫的制取、检验、收集和尾气处理,不能达到相应实验目的是( )
| A. | 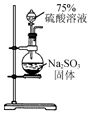 用装置制取二氧化硫 | B. | 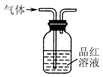 用装置检验二氧化硫的漂白性 | ||
| C. | 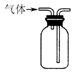 用装置收集二氧化硫 | D. | 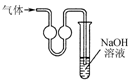 用装置进行尾气处理 |