题目内容
某溶液中含有Ba2+、HCO3-、Cl-、NO3-四种离子,先向溶液中加入足量NaOH,再加入足量稀盐酸;溶液中大量减少的离子是( )
| A、Ba2+ |
| B、Cl- |
| C、HCO3- |
| D、NO3- |
考点:离子共存问题,离子反应发生的条件
专题:
分析:根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,以此来解答.
解答:
解:某溶液中含有Ba2+、HCO3-、Cl-、NO3-四种离子,先向溶液中加入足量NaOH,能发生反应的离子反应为HCO3-+OH-=H2O+CO32-,再加入足量稀盐酸,发生的反应为OH-+H+=H2O,氯离子增加,钡离子、硝酸根离子数目不变,可知大量减少的离子为HCO3-,
故选C.
故选C.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
已知下列三个数据:7.2×10-4、4.6×10-4、4.9×10-10它们分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2═HCN+NaNO2、NaCN+HF═HCN+NaF、NaNO2+HF═HNO2+NaF.下列叙述正确的是( )
| A、K(HF)=7.2×10-4 |
| B、K(HNO2)=4.9×10-10 |
| C、HF>HNO2>HCN |
| D、无法判断酸性强弱顺序 |
25℃时,将一定浓度的盐酸和一定浓度的氨水按2:1 的体积比混合,若混合溶液中c(NH4+)=c(Cl-),则溶液的pH( )
| A、大于7 | B、小于7 |
| C、等于7 | D、无法确定 |
下列关于容量瓶的说法不正确的是( )
| A、容量瓶上一般标有规格、温度和刻度线 |
| B、容量瓶在使用前要检查是否漏水 |
| C、可将固体或浓溶液直接在容量瓶中溶解或稀释 |
| D、容量瓶不能加热,也不宜长时间储存所配溶液 |
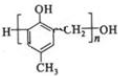 ,化合物C和化合物N的合成路线如下
,化合物C和化合物N的合成路线如下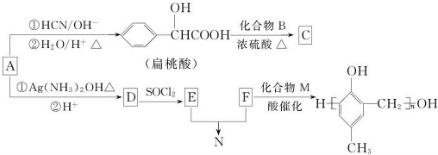
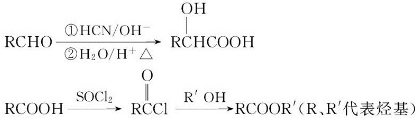
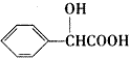 )有多种同分异构体.其中含有三个取代基,能与FeCl3溶液发生显色反应,也能与NaHCO3溶液反应放出气体的同分异构体共有
)有多种同分异构体.其中含有三个取代基,能与FeCl3溶液发生显色反应,也能与NaHCO3溶液反应放出气体的同分异构体共有