��Ŀ����
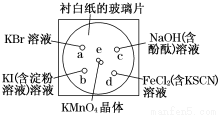
��ѧʵ����ͻ�����Ч�ؼ�����Ⱦ��ʵ�ֻ�ѧʵ����ɫ����Ҫ��ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1 mol/L��KBr��KI(��������Һ)��NaOH(����̪)��FeCl2(��KSCN)��Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ��(����ͼ��ʾ)����Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻá�(e����Ӧ�Ļ�ѧ����ʽΪ��2KMnO4��16HCl===2MnCl2��5Cl2����8H2O)
��1��e����Ӧ�б�������HCl��μӷ�Ӧ��HCl�����ʵ���֮��Ϊ ��
��2��b����ʵ������Ϊ___________________________________��
��3��c����Ӧ�Ļ�ѧ����ʽΪ_____________________________________����״���£�����0.224 L Cl2��NaOH��Һ���պ�ת�Ƶ��ӵ����ʵ���Ϊ mol��
��4��ͨ����ʵ��Ƚ�Cl2��FeCl3��KMnO4����������������ǿ������˳���� ��
��1�� 5��8
��2����Һ����ɫ��Ϊ��ɫ
��3��Cl2��2NaOH===NaCl��NaClO��H2O 0.01
��4��KMnO4��Cl2��FeCl3
��������
���������e����Ӧ�Ļ�ѧ����ʽΪ��2KMnO4��16HCl===2MnCl2��5Cl2����8H2O���ʱ�������HCl��μӷ�Ӧ��HCl֮��Ϊ10:16=5��8��e������Cl2��Cl2����b��������Ӧ��Cl2 +2I��== I2+2Cl������b������Ϊ��Һ����ɫ��Ϊ��ɫ��Cl2����c��Cl2��NaOH������ӦCl2��2NaOH===NaCl��NaClO��H2O����״���£�����0.224 L Cl2��NaOH��Һ���պ�ת�Ƶ��ӵ����ʵ���Ϊ0.01mol��Cl2����d����Fe2+������Ӧ��Cl2+ 2Fe2+=2Cl��+2Fe3+����Cl2��FeCl3��KMnO4����������������ǿ������˳����KMnO4��Cl2��FeCl3��
���㣺�����Ʊ������ʷ�Ӧ��������ԭ��Ӧԭ����

�����±��ṩ�����ݣ��ж��������ӷ���ʽ��ѧ����ʽ��ȷ����
��ѧʽ | ���볣�� |
HClO | K=3��10-8 |
H2CO3 | K1=4��10-7 |
K2=6��10-11 |
A����Na2CO3��Һ�еμ�������ˮ��CO32��+2Cl2+H2O = 2Cl �� + 2HClO + CO2��
B����NaHCO3��Һ�еμ�������ˮ��2HCO3��+Cl2 = Cl �� +ClO �� +2CO2��+ H2O
C����NaClO��Һ��ͨ����CO2��CO2 + NaClO + H2O= NaHCO3 + HClO
D����NaClO��Һ��ͨ����CO2��CO2 + 2NaClO + H2O = Na2CO3 + 2HClO